下列有关说法正确的是( )
| A.大多数金属在自然界以游离态形式存在 |
| B.工业上,一般用热还原法获得Hg和Ag |
| C.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸 |
| D.人们常用钢作建造材料而不用纯铁主要原因是钢的机械性能更好 |
某FeSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6 mol·L-1,则此溶液最多可溶解铁粉的质量为
| A.11.2 g | B.16.8 g | C.19.6 g | D.22.4 g |
已知25℃时,有关弱酸的电离平衡常数:
| 弱酸 |
CH3COOH |
HCN |
H2CO3 |
| 电离平衡常数 |
1.8×10-5 |
4.9×10-10 |
K1=4.3×10-7 K2=5.6×10-11 |
则下列有关说法不正确的是
A.25℃时,0.1mol·L-1各溶液的pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B.25℃时,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)相等
C.25℃时,若同浓度的醋酸和氢氧化钠等体积混合,所得溶液pH=8,则
c(Na+)-c(CH3COO-)=9.9×10-7 mol·L-1
D.NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
已知101 k Pa时辛烷的燃烧热为-5518 kJ· mol-1。则下列热化学方程式书写正确的是
| A.2C8H18 + 25O2 = 16CO2 + 18H2O△H =-11036 kJ·mol-1 |
| B.2C8H18(l) + 25O2(g) = 16CO2(g) + 18H2O(l)△H =-11036 kJ·mol-1 |
| C.2C8H18(l) + 25O2(g) = 16CO2(g) + 18H2O(g)△H =-11036 kJ·mol-1 |
| D.2C8H18(l) + 25O2(g) = 16CO2(g))+18H2O(l)△H =-5518kJ·mol-1 |
海洋中蕴藏着丰富资源,对它的开发利用有利于缓解当前资源紧张的困局,工业上从海水中提取的某些无机物的简易流程可以用下图表示: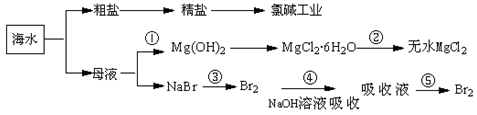
下列有关说法不正确的是
| A.氯碱工业中采用阳离子交换膜电解槽,可以防止氯气与碱的反应 |
| B.第②步中结晶出的MgCl2·6H2O不能采用直接在空气中受热分解制无水MgCl2 |
| C.第①步常采用往母液中加浓NaOH溶液来获取Mg(OH)2 |
| D.从第③步到第⑤步的目的是获得含溴单质浓度较高的溶液 |
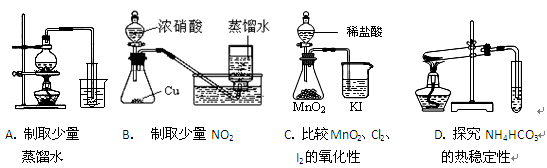
下列实验方案正确且能达到相应实验预期目的的是