已知:①相同温度下溶解度:MgCO3:0.02g/100g水,Mg(OH)2:0.0009g/100g 水;
② 时,亚磷酸(
时,亚磷酸( ,二元酸)的
,二元酸)的 ,
, ;
;
草酸( )的
)的 ,
,
③相同条件下电离出S2-的能力:FeS>H2S>CuS,以下离子方程式错误的是( )
| A.Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O |
B. |
C. |
D. |
有BaCl2和KCl的混合溶液V L,将它分成两等份。一份滴加稀硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀。反应中消耗m m ol H2SO4、n mol AgNO3。据此得知原混合溶液中的K+的物质的量浓度为( )
A.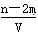 mol·L-1 mol·L-1 |
B. mol·L-1 mol·L-1 |
C. mol·L-1 mol·L-1 |
D.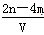 mol·L-1 mol·L-1 |
共 价键的断裂有均裂和异裂两种方式,即均裂:A∶B→A·+B·,
异裂:A∶B→A++[∶B]-。下列 化学反应中发生共价键均裂的是
| A.2K+2H2O=== 2KOH+H2↑ | B.2Na+2C2H5OH―→2C2H5ONa+H2↑ |
| C.HCl+NaOH ===" NaCl" + H2O | D.CH3COOH+C2H5OH H2O+CH3COOC2H5 H2O+CH3COOC2H5 |
下列关于元素的叙述正确的是
| A.金属元素与非金属元素能形成共价化合物 |
| B.只有在原子中,质子数才与核外电子数相等 |
| C.目前使用的元素周期表中,最长的周期含有36种元素 |
| D.非金属元素形成的共价化合物中,原子的最外层电子数只能是2或8 |
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如 右图转化关系(部分生成物和反应条件略去)。下列推断不正确的是
A.若X是Na2CO3,C为CO2,则A一定是氯气,且D和E不反应
B.若A是单质,B和D的反应是OH-+HCO3- =H2O+ CO32-,则E一定能还原Fe2O3
C.若D为CO,C能和E反应,则A一定为Na2O2
D.若D为白色沉淀,与A摩尔质量相等,则X一定是铝盐
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是
| A.元素原子的最外层电子数等于元素的最高化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 |
| D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |