我国青海湖采集的天然碱样品可表示为aNa2CO3·bNaHCO3·cH2O(a、b、c为最简整数比)。小红同学为测定其组成,称取该天然碱样品16.6g进行如下实验:
已知:1.碳酸钠比较稳定,加热时不分解 ;2. 2NaHCO3 Na2CO3 +CO2 ↑ +H2O
Na2CO3 +CO2 ↑ +H2O
3.图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
实验步骤
实验时,组装好装置,实验前应先 ,然后,实验步骤是:
① 反复推拉注射器 ② 称量E、F的质量 ③ 关闭弹簧夹,加热D处试管直到反
应不再进行 ④ 打开弹簧夹,再次反复缓缓推拉注射器 ⑤ 再次称量E、F的质量。
(二)问题探究:
(2) E中的药品为 ,E的作用是 。C、F、G中装有碱石灰(生石灰与烧碱的固体混合物),则C的作用是 , F的作用是 。写出 F装置中所发生反应的一个化学方程式 。
(3)实验步骤②与③能否颠倒 (填“能”或“不能”)。若不进行步骤④的操作,则所测得的碳酸氢钠质量 (填“偏大”、“偏小”、“无影响”), 该操作中推注射器时缓缓的目的是 ;若没有G装置,则碳酸氢钠的质量 (填“偏大”、“偏小”、“无影响”)。
(4)下表是实验记录数据:
| 反应前 |
反应后 |
| E的质量为100.0g |
E的质量为102.25g |
| F的质量为50.0g |
F的质量为51.1g |
则: ① 碳酸氢钠分解生成二氧化碳的质量为 g
② 碳酸氢钠的质量为 g
③ 该天然碱的化学式中a:b:c= 。
2020年年初新冠状病毒在我国传播扩散,给我们的生命健康和生产带来严重影响。预防新冠状病毒的主要措施有戴口罩、勤洗手、养成良好饮食习惯、减少聚集等。在抗击新冠状病毒的过程中,我们也学到了不少防疫新冠状病毒的知识。
(1)医用口罩。
医用口罩是由三层无纺布做成的。中间一层用来隔离病毒的喷熔无纺布的材料是聚丙烯。聚丙烯和聚乙烯一样都属于 高分子材料(选填“合金”“复合”“合成”“天然”)。口罩隔离病毒相当于化学实验操作中的 (填写实验操作名称)。
(2)良好的饮食习惯。
营养要全面、均衡。要多吃富含蛋白质、维生素以及矿物质的食物,比如肉、蛋、奶类、新鲜的水果和蔬菜以及坚果等。
樱桃是人们喜爱的一种水果,富含糖类、蛋白质、维生素(A、B、C等)、矿物质(钙、磷、铁等),具有很高的营养价值。樱桃所含的营养成分中,能够提供能量的是 、蛋白质。樱桃中含有的钙、磷、铁等,是指 (填“分子”“原子”“元素”)。
(3)正确使用消毒液。
某品牌消毒液的有效成分主要是乙醇(体积分数72%﹣82%)、过氧化氢(0.10%﹣0.14%( ))。乙醇俗名 ,乙醇消毒液在使用过程中要特别注意远离火源,其原因是乙醇具有挥发性、 性,请写出乙醇燃烧的化学方程式 。
洁厕灵(含HCl)、84消毒液(含NaClO)是生活中两种常见的清洁、消毒用品;两者混合使用时会发生化学反应(2HCl+NaClO═NaCl+H2O+Cl2↑),生成有毒物质,因此禁止将两者混合使用!下列说法正确的是 。
A.Cl2是有毒气体
B.洁厕灵可以用铁质容器盛放
C.洁厕灵可用于清洁大理石台面
D.室内喷洒84消毒液后,会嗅到刺激性气味,是因为微粒在不断运动
E.口服84消毒液可以预防新冠状病毒
如图中A~G和M均是初中化学常见物质,①~⑥是初中常见的不同化学反应的编号,A是碳酸氢钠,B、E是组成元素相同的物质,G是铁锈的主要成分,H、M是常见的碱。“→”表示物质间有转化关系,图中部分反应条件和反应物、生成物已省略。请回答下列问题:
(1)写出反应③的化学方程式 。
(2)物质C的化学式是 。
(3)反应①~⑥不涉及的基本反应类型是 反应。

“久大盐化”是四川遂宁的重点企业,其生产的食盐是重要的调味品。绿色应用是化工生产的发展方向。为了除去NaCl溶液中含有的少量MgCl2、CaCl2和Na2SO4,某小组同学选用Na2CO3溶液、稀盐酸、Ba(OH)2溶液三种试剂,按一定顺序进行如图所示的实验。回答下列问题:
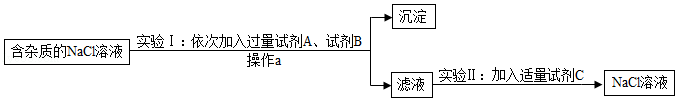
(1)操作a的名称是 。
(2)实验Ⅰ中加入的试剂B是 。(填序号)
①稀盐酸
②碳酸钠溶液
③氢氧化钡溶液
(3)实验Ⅱ中发生中和反应的化学方程式是 。
化学就在我们身边,生活中蕴藏着丰富的化学知识。
(1)妈妈为了让小宇身体更健康,给她买了某品牌的保健品,标签部分信息如下:
|
产品名称:XX牌XX口服液 主要原料:…… 功效成分及含量:每支含:钙86.6mg,铁3.14mg,锌3.04mg,硒6.999μg…… |
这里钙、铁、锌、硒指的是 。(选填“原子”、“分子”、“物质”、“元素”)
(2)均衡膳食,保持良好的饮食习惯,就能满足健康成长的需要,不必刻意用保健品来补充。某天,妈妈准备的午餐如下:米饭、红烧肉、排骨汤、炸鸡腿。从均衡营养的角度看,这份午餐还缺少的营养素是 (填字母编号)。
A.糖类
B.蛋白质
C.油脂
D.维生素
(3)妈妈炒菜的铁锅、烧水的铝壶都属于 材料。(选填“金属”、“无机非金属”、“有机高分子”、“复合材料”)
如图是A、B、C三种固体物质(均不含结晶水)的溶解度曲线。请回答下列问题:
(1)在 ℃时,A、C的溶解度相同。
(2)A中混有少量B,提纯A的方法是 结晶。
