常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-,横坐标表示加入NaOH的体积)。根据图示判断,下列说法正确的是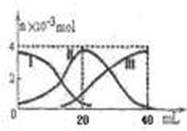
| A.当V(NaOH)=40mL时,c (Na+)+ c(H+)="2" c(A2-)+c(OH-) |
| B.当V(NaOH)=20mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
| C.滴加过程中当溶液呈中性时,V(NaOH)<20mL |
| D.HA-的电离程度小于水解程度 |
有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同。下列事实不能说明上述观点的是:
| A.苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 |
| B.甲苯能使酸性高锰酸钾溶液褪色,乙烷不能使酸性高锰酸钾溶液褪色 |
| C.乙烯能发生加成反应,乙烷不能发生加成反应 |
| D.苯与硝酸加热时发生取代反应,甲苯与硝酸常温下就能发生取代反应 |
下列有关利用乙醛制备银镜过程的说法不正确的是
| A.边振荡盛有2%的AgNO3溶液的试管,边滴入2%的氨水至最初的沉淀恰好溶解为止 |
| B.将几滴银氨溶液滴入2 mL乙醛中 |
| C.将盛有乙醛与银氨溶液混合液的试管置于热水浴中加热 |
| D.在银氨溶液的配制过程中溶液pH增大 |
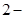 甲基
甲基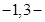 丁二烯和等物质的量的溴发生加成反应,其加成产物中二溴代烃有
丁二烯和等物质的量的溴发生加成反应,其加成产物中二溴代烃有
| A.一种 | B.二种 | C.三种 | D.四种 |
下列离子方程式正确的是
A.过量乙酸与碳酸钠溶液反应:2H++CO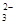 == CO2↑+ H2O == CO2↑+ H2O |
| B.溴乙烷在NaOH水溶液中加热: CH3CH2Br + NaOH →CH2=CH2↑+NaBr + H2O |
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O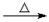 2C6H5OH+CO 2C6H5OH+CO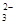 |
D.甲醛溶液与足量的银氨溶液共热:HCHO+4[Ag(NH3)2]++4OH-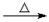 CO CO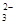 +2NH +2NH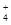 +4Ag↓+6NH3+2H2O +4Ag↓+6NH3+2H2O |
下列叙述正确的是
| A.甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色 |
B.有机物  的消去产物有两种 的消去产物有两种 |
| C.有机物A(C3H6O2)能发生加聚反应,可推知A的结构一定是CH2=CH—COOCH3 |
| D.可用溴水鉴别直馏汽油、四氯化碳和乙酸 |