在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、NO3-、Cl-,该溶液放在用惰性电极材料做电极的电解槽中,通电片刻,则氧化产物与还原产物质质量比为…( )
| A.35.5:108 | B.16:207 | C.8:1 | D.108:35.5 |
解释下列现象的离子方程式不正确的是
| A.铁溶于稀硝酸,溶液变黄: 3 Fe +8H+ +2NO3-="3" Fe2++2NO+4H2O |
| B.FeBr2与Cl2物质的量之比为1∶1时:2Fe2++2Br-+2Cl2=2Fe3++4C1-+Br2 |
| C.向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:A13++2SO42-+2Ba2++4OH-=2BaSO4↓+A1O2-+2H2O |
| D.漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3C1O-+3H2O=Fe(OH)3↓+3HC1O |
下列实验方案正确且能达到相应实验预期目的且安全的是
下列事实解释准确的是
| A.糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。脱氧过程中铁作原电池正极,电极反应为: Fe-2e- = Fe2+ |
| B.酸性氢氧燃料电池的正极电极反应为: 2H2O十O2+4e-=4OH- |
| C.用石墨电极电解CuC12溶液:阳极上发生的反应:2C1-—2e一=C12↑ |
| D.铅蓄电池的正极反应为:PbO2 +4H+ +2e一=Pb2+ +2H2O |
已知温度T时,水的离子积常数为KW,该温度下将V1mL a mol/L的一元酸HA与V2mL b mol·L-1的一元碱BOH充分混合,下列判断一定正确的是
A.若V1a=V2b,稀释此混合溶液时,溶液中各离子浓度一定都发生变化
B.若pH( HA)+pH(BOH) =14,则V1=V2时,酸碱恰好完全中和
C.此混合液中: c( H+)+c(B+) ≤ c(OH一)+c(A一)
D.若混合溶液中。c(OH一) =√KWmol·L-1,则此溶液一定呈中性
如图所示,夹子开始处于关闭状态,将液体A滴人烧瓶与气体B充分反应,打开夹子,可发现试管内的水立刻沸腾了,则液体 A和气体B的组合不可能是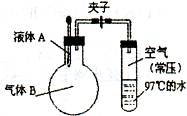
| A.水、氯化氢 |
| B.硫酸、氨气 |
| C.氢氧化钠溶液、二氧化硫 |
| D.氢氧化钠溶液、一氧化碳 |