已知:(1)2Fe3++2I-=2Fe2++I2 (2)Br2+2Fe2+=2Fe3++2Br-由此推断氧化剂的氧化性强弱顺序为
| A.Br2>Fe3+>I2 | B.Fe3+>Br2>I2 | C.I2>Br2>Fe3+ | D.Br2>I2>Fe3+ |
阴离子Xn-含中子N个,X的质量数为A,则a g X的氢化物中含质子的物质的量是
A.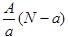 mol mol |
B.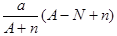 mol mol |
C.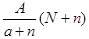 mol mol |
D. mo1 mo1 |
下列各项表达中正确的是
A. 的电子式为 的电子式为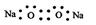 |
B.16g甲烷完全燃烧生成的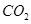 为11.2L(标准状况) 为11.2L(标准状况) |
| C.在氮原子中,质子数为7而中子数不一定为7 |
D.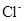 的结构示意图为 的结构示意图为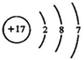 |
下列关于C、Si、S、Cl四种非金属元素的说法中,正确的是
A.在自然界中都能以游离态存在
B.两两结合形成的化合物都是共价化合物
C.氢化物的热稳定性比较:CH4 < SiH4 < H2S < HCl
D.最高价氧化物都能与水反应生成相应的酸,且酸性依次增强
标准状况下,气态分子断开1mol化学键所需的能量称为键能。已知H—H,H—O,和O==O键的键能分别为436KJ/mol,463KJ/mol,495KJ/mol,下列热化学方程式正确的是
| A.H2O(g)==H2(g)+1/2O2(g) △H =—485KJ/mol |
| B.H2O(g)==H2(g)+1/2O2(g) △H =" +" 485KJ/mol |
| C.2 H2(g) + O2(g)="=2" H2O(g) △H =" +" 485KJ/mol |
| D.2 H2(g) + O2(g)="=2" H2O(g) △H =—485KJ/mol |
aXn-和bYm+为短周期两元素的离子, 它们的电子层结构相同, 下列判断错误的是
| A.原子半径X<Y | B.a+n=b-m |
| C.Y最高价氧化物的化学式为YOm | D.X的氢化物的化学式为HnX |