X、Y、Z、W是中学化学中常见的四种元素,它们的原子序数依次增大。化学式为W3Y4的物质具有磁性。X的单质在Y2中燃烧可生成化学式为XY和XY2的两种气体。Z的单质是金属,它与金属钾可作为原子反应堆的导热剂,且该导热剂常温下是液体。下列有关说法中错误的是
| A.W3Y4的化学式为Fe3O4 | B.Z在常温下是固体 |
| C.XY和XY2分别是NO和NO2 | D.W原子的基态电子排布式为[Ar]3d64s2 |
(10分)下图表示各物质之间的转化关系。已知A、D、F、H均为单质,X常温下为液体,B为淡黄色固体,J溶于酸得到黄色溶液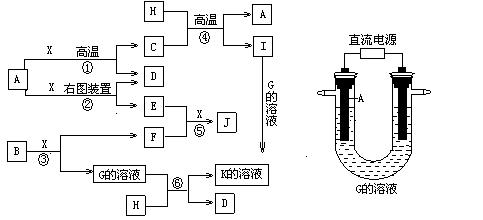
请按要求填空:
(1)写出生成E的电极反应式:
反应⑤的现象是: ___________________
(2)反应①的化学反应方程式:
在实验室中引发反应④的操作是:
(3) I和G溶液反应的化学方程式:
工业上处理含Cr2O72—的酸性工业废水用以下方法:①往工业废水中加入适量的NaCl,搅拌均匀;②用Fe为电极进行电解,经过一段时间有Cr(OH)3和Fe(OH)2沉淀产生;过滤回收沉淀,废水达到排放标准。试回答: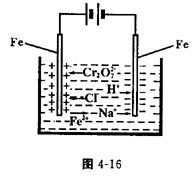
⑴ 电解时的电极反应:
阳极_____________________,阴极______________。
⑵ Cr2O72-转变成Cr3+的离子反应方程式
⑶能否用Cu电极来代替Fe电极?______________(填“能”或“不能”),简述理由。
铅蓄电池是典型的可充型电池,它的正负极板是惰性材料,电池总反应式为: Pb+PbO2+4H++2SO42-2PbSO4+2H2O
Pb+PbO2+4H++2SO42-2PbSO4+2H2O
回答下列问题(不考虑氢、氧的氧化还原)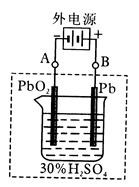
(1)放电时:正极的电极反应式是;电解液中H2SO4的浓度将变________,当外电路通过1.5mol电子时,理论上负极板的质量增加_______________g。
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成__________,B电极上生成________,此时铅蓄电池的正负极的极性将____________。
1mol二氧化氮和1mol三氧化硫肯定有相同的…………………………………()
| A.体积 | B.原子数 | C.分子数 | D.质量 |
把标准状况下4.48 L的CO2通过一定量的固体Na2O2后,收集到标准状况下3.36 L气体。则这3.36 L气体的质量是……………………………………………………()
| A.6.0 g | B.4.8 g | C.3.2 g | D.5.6 g |