下列说法正确的是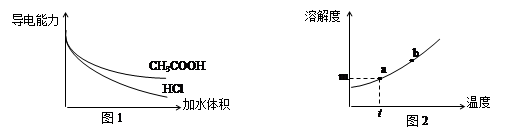
| A.图1表示pH相同的盐酸和醋酸加水稀释时溶液导电能力的变化 |
| B.图1表示物质的量浓度相同的盐酸和醋酸加水稀释时溶液导电能力的变化 |
| C.图2中,t ℃时饱和溶液的质量分数为m% |
| D.图2中,若保持温度不变,可以通过增加溶质的方法使溶液从a点变为b点 |
根据下列反应判断有关物质还原性由强到弱的顺序是
①H2SO3+I2+H2O═2HI+H2SO4
②2FeCl3+2HI═2FeCl2+2HCl+I2
③3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
| A.H2SO3>I﹣>Fe2+>NO |
| B.I﹣>Fe2+>H2SO3>NO |
| C.Fe2+>I﹣>H2SO3>NO |
| D.NO>Fe2+>H2SO3>I﹣ |
某溶液中只含有Na+、Al3+、Cl﹣、SO42﹣ 四种离子,已知前三种离子的个数比为3:2:1,则溶液中Al3+和 SO42﹣的离子个数比为
| A.1:2 | B.1:4 | C.3:4 | D.3:2 |
将标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为bg/mL,则该盐酸的物质的量浓度是
A.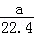 mo1•L﹣1 mo1•L﹣1 |
B.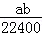 mol•L﹣1 mol•L﹣1 |
C.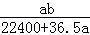 mol•L﹣1 mol•L﹣1 |
D.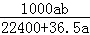 mol•L﹣1 mol•L﹣1 |
已知3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O,则下列说法不正确的是
| A.Cu作还原剂,HNO3作氧化剂 |
| B.HNO3在该反应中只有部分表现出了氧化性 |
| C.每生成22.4L(标准状况)NO有3mol的电子转移 |
| D.如果有8molHNO3被还原,则生成了2molNO |
下列反应中,不是氧化还原反应的是
①H2+Cl2 2HCl ②Na2CO3+2HCl═2NaCl+H2O+CO2↑
2HCl ②Na2CO3+2HCl═2NaCl+H2O+CO2↑
③2H2O 2H2↑+O2↑④CuO+2HNO3═Cu(NO3)2+H2O
2H2↑+O2↑④CuO+2HNO3═Cu(NO3)2+H2O
⑤2HgO 2Hg+O2↑
2Hg+O2↑
| A.②④ | B.①③ | C.①②③ | D.④⑤ |