互为同分异构体的有机物A、B、C的分子式均为C5H8O2,其中A为直链结构,加热时能与新制的氢氧化铜浊液反应,生成砖红色物质;A分子中核磁共振氢谱图中有三组峰,且峰面积之比为2:1:1。B为五元环酯。C的红外光谱表明其分子中存在甲基。A~I等有机物的转化关系如下:
已知:烯烃在一定条件下可与卤素单质发生a—H原子的取代反应。
(1)A、B的结构简式分别是:A ,B 。
(2)C为反式结构,其结构式为 。
(3)写出下列反应的化学方程式;
D→C: 。
G→H: 。
(4)写出下列反应类型:
F→G ,A→I中的① 。
(5)写出F发生加聚反应生成的产物的结构简式 。
(6)与A的官能团组成和个数均相同的同分异构体
还有 个。
O2和O3是氧元素的两种单质,根据其分子式完成下列各题:
(1)等质量的O2和O3所含分子个数比为,原子个数比为,分子的物质的量之比为。
(2)等温等压下,等体积的氧气和臭氧所含分子个数比为,原子个数比为,质量之比为。
(3)设NA为阿伏加德罗常数的数值,如果a g氧气中含有的分子数为b,则c g氧气在标准状况下的体积约是(用含NA的式子表示)。
(4)将8 g SO3加入Χg 水中,所形成的溶液里SO42-和水分子个数之比为1:5,则Χ等于。
(5)常温常压下,14 g由N2和CO组成的混合气体中含有的原子数目为。
选择下列实验方法分离物质,将分离方法的序号填在横线上:
A 过滤 B.结晶 C.分液 D.蒸馏 E.萃取分液 F.升华 G.渗析
(1)分离水和苯的混合物;
(2)分离饱和氯化钾溶液和沙子的混合物;
(3)从硝酸钾和氯化钠的混合溶液中获得硝酸钾;
(4)分离酒精(沸点为78.1℃)和甲苯(沸点为110.6℃)的混合物;
(5)从碘水中提取碘单质。
某些元素的性质或原子结构信息如下表所示(每空2分,共16分).:
| A(短周期) |
B(短周期) |
C |
D(短周期) |
| 原子最外层上p电子数等于次外层电子数 |
原子最外层有两个未成对电子,其单质为人类生存必需物质 |
单质为生活中常见的金属材料,有紫红色金属光泽 |
单质是常见的半导体材料,广泛应用于IT行业 |
(1)写出A单质与浓硝酸加热反应的化学方程式:。
(2)写出B元素在周期表中的位置:,
写出C元素基态原子的电子排布式:_。
(3)写出A与D的氧化物在高温下反应的化学方程式:_。
(4)写出B、D形成的化合物与NaOH溶液反应的离子方程式:。
(5)比较A、B、D三种元素原子的第一电离能的大小(由大到小用元素符号表示)。
(6)等电子原理——原子总数相同、价电子总数相同的粒子具有相似的化学键特征,它们的许多性质是相近的。写出二种由多个原子组成的含有与N3-电子数相同的粒子 (分子离子各一种)的化学式、。这些粒子空间构型为 。
(每空2分,共16分).已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC为离子化合物,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为产生温室效应的主要气体。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24, ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2∶1,三个氯离子位于外界。请根据以上情况,回答下列问题:(答题时A、B、C、D、E用所对应的元素符号表示)
(1)A、B、C的第一电离能由小到大的顺序为。
(2)B的氢化物分子的立体构型是其中心原子采取_杂化。
(3)写出化合物AC2的电子式;一种由B、C组成的化合物与AC2互为等电子体,其化学式为。
(4) E的核外电子排布式是__,ECl3形成的配合物的化学式为。
(5)B的最高价氧化物对应的水化物的稀溶液与D的单质反应时,B被还原到最低价,该反
应的化学方程式是
下表列出了前20号元素中的某些元素性质的有关数据(每空2分,共14分).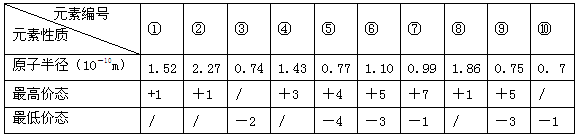
试回答下列问题:
(1)以上10种元素的原子中,失去核外第一个电子所需能量最少的是(填编号)。
(2)上述⑤、⑥、⑦三种元素中的某两种元素形成的化合物中,每个原子都满足最外层为8电子稳定结构的物质可能是(写分子式)。某元素R的原子半径为1. 02×10-10m,该元素在周期表中位于;若物质Na2R3是一种含有非极性共价键的离子化合物,请你写出该化合物的电子式。
(3)元素⑤的某种单质具有平面层状结构,同一层中的原子构成许许多多的正六边形,此单质与熔融的②单质相互作用,形成某种青铜色的物质(其中的元素②用“●”表示),原子分布如图所示,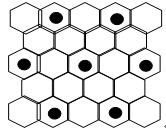
该物质的化学式为。
(4)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
①下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是_____(请用相应的编号填写)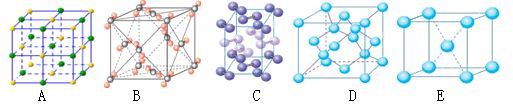
②将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝色的配合离子。请写出生成此配合离子的离子方程式:。