在相同温度时,100mL 0.01mol·L-1的醋酸溶液与10mL 0.1mol·L-1的醋酸溶液相比较,下列数值中,前者大于后者的是
| A.H+的物质的量 | B.醋酸的电离常数 |
| C.中和时所需NaOH的量 | D.CH3COOH的物质的量 |
铁镍蓄电池,放电时的总反应为: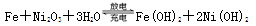 下列有关该电池的说法不正确的是
下列有关该电池的说法不正确的是
| A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B.电池放电时,负极反应为Fe+2OH--2e-===Fe(OH)2 |
| C.电池充电过程中,阴极附近溶液的pH降低 |
| D.电池充电时,阳极反应为2Ni(OH)2+2OH--2e-===Ni2O3+3H2O |
将等质量的两份锌粉a、b分别加入过量的稀硫酸,同时向a中加少量CuSO4溶液,下图中产生H2的体积V(L)与时间t(min)的关系,其中正确的是
在铝—铜—浓硝酸原电池中,当导线中有1mol电子通时,理论上的两极变化是
①铝片溶解9g②铜片溶解32g③铜片上析出1 gH2 ④铝片上析出1mol NO2
| A.①③ | B.①④ | C.②③ | D.②④ |
发射“嫦娥一号”月球探测卫星的长征三号甲运载火箭的第三子级使用的燃料是液氢和液氧,已知下列热化学方程式:
①H2(g)+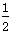 O2(g)=H2O(l) ΔH1=-285.8 kJ/mol
O2(g)=H2O(l) ΔH1=-285.8 kJ/mol
②H2(g)=H2(l) ΔH2=-0.92 kJ/mol
③O2(g)=O2(l) ΔH3=-6.84 kJ/mol
④H2O(l)=H2O(g) ΔH4=+44.0 kJ/mol
则反应H2(l)+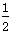 O2(l)=H2O(g)的反应热ΔH为
O2(l)=H2O(g)的反应热ΔH为
| A.+237.46 kJ/mol | B.-474.92 kJ/mol |
| C.-118.73 kJ/mol | D.-237.46 kJ/mol |
反应A(g)+3B(g) 2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是
2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是
A.v(A)=0.15 mol·L-1·min-1
B.v(B)=0.015 mol·L-1·s-1
C.v(C)=0.40 mol·L-1·min-1
D.v(D)=0.45 mol·L-1·min-1