科学探究是奇妙的过程,请你一起参与并填写下列空白。
【提出问题】小森同学在滴加FeCl3溶液时,不小心把滴加FeCl3溶液的滴管放入到盛“双
氧水”(过氧化氢)的试剂瓶中,发现有大量的气泡产生。小森联想到用二氧化锰可作为过氧化氢的催化剂,他想FeCl3溶液能否也可以作为过氧化氢分解的催化剂呢?于是他做了以下探究。
【猜想与假设】FeCl3溶液能作过氧化氢分解的催化剂
【设计与实验】
| 实验步骤 |
实验现象 |
实验结论 |
| 在一支试管中加入5mL15%的H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管 |
|
FeCl3溶液可以催化分解H2O2 |
【讨论与反思】
已知FeCl3溶液中含有H2O 、Fe3+和Cl-三种微粒,小森同学又做了三种猜想:
猜想1:真正催化分解H2O2的是FeCl3溶液中的H2O
猜想2:真正催化分解H2O2的是FeCl3溶液中的Fe3+
猜想3:真正催化分解H2O2的是FeCl3溶液中的CI—
你认为最不可能的是哪一种猜想, 。小森同学认为,要验证猜想,至少还需要做 个对比实验。
带火星的木条在氧气中可以复燃。那么,是不是只有纯净的氧气才能使带火星的木条复燃呢?为此,同学们开展了相关的实验探究。实验主要步骤如下:先制取一定量的氧气备用,再测得集气瓶实际容积为317 mL,然后采用某种正确的收集方法得到5瓶氧气含量不同的空气,最后用带火星的木条来检验,观察木条是否复燃。相关的数据见下表:
| 集气 瓶编号 |
瓶内预装水体积/mL |
充入氧气体积/mL |
瓶内空气体积/mL |
瓶内空气里氧气的体积分数 |
木条能 不能复燃 |
| 1 |
120 |
120 |
197 |
50.9% |
能 |
| 2 |
97 |
97 |
220 |
能 |
|
| 3 |
90 |
90 |
227 |
43.4% |
能 |
| 4 |
84 |
84 |
233 |
41.9% |
能 |
| 5 |
81 |
81 |
236 |
41.2% |
不能 |
(1)试将上表空白处补充完整(保留一位小数)。
(2)由该实验可得到的结论是。
某校研究性学习小组进行测定空气里氧气的含量的实验,大家分别对课本上的实验进行了相应的改进。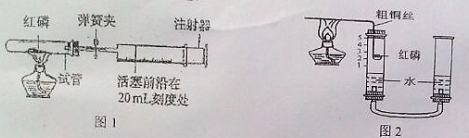
(1)甲同学采用了图1所示装置:选用实际容积为40mL的试管作反应容器,将过量的红磷放入试管,用橡皮塞塞紧试管口,通过导管与实际容积为60mL的针筒注射器(摩擦系数很小)组成如图1的实验装置。假设此实验能按照甲同学的设想正常进行,且红磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
①实验前,甲同学打开弹簧夹,将注射器的活塞前沿从20mL刻度处推至15mL刻度处,然后松手,发现活塞仍能返回至20mL刻度处,甲同学这样操作的目的是为了;
②红磷燃烧的符号表达式为;
③若先夹紧弹簧夹,待红磷充分燃烧结束,试管冷却后再打开弹簧夹,最终注射器活塞前沿停在示
数mL处;
④若不使用弹簧夹,用酒精灯加热红磷,充分反应直至燃烧结束,试管冷却。注射器活塞的变化是。
(2)乙同学采用了图2所示装置:通过粗铜丝来点燃玻璃棺内的红磷,这利用了金属铜的性。在该实验中,水的作用是(选填序号)
①吸收生成物,防止污染; ②加速冷却; ③缓冲气压
某实验小组用排水法收集一瓶呼出的气体,把一根燃着的木条伸入瓶内,很快熄灭了。据此,对呼出气体的成分,同学们提出了下列假设:
A认为是二氧化碳 B认为是氮气 C认为是二氧化碳和氮气的混合物
为了弄清它的真实成分,大家设计了下列实验:(已知二氧化碳能溶于水)
| 实验步骤与内容 |
实验现象 |
结论 |
| (1)去一瓶呼出的气体,倒入足量的澄清石灰水后,立即盖上玻璃片振荡 |
呼出气体中含有二氧化碳 |
|
| (2)把步骤(1)中的集气瓶倒立在水槽中,并在水下拿开玻璃片 |
瓶内液体上升至一定高度后便不再改变 |
瓶内剩余气体溶于水 |
| (3)把步骤(2)中的集气瓶取出,向瓶内插入一根燃着的木条 |
木条立即熄灭 |
瓶内剩余气体不支持燃烧 |
能否由上述实验确定呼出气体中是否含有水蒸气(填“能”或“否”);
综上所述,你得出的结论是:假设(填字母序号)成立。
(17分)下面是学习化学第二单元课题3后,进行“氧气的性质”的探究,请回答: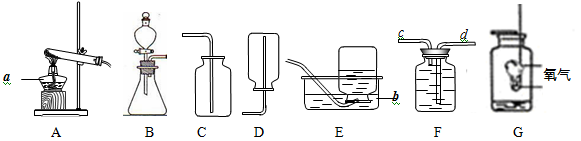
(1)写出图中仪器的名称a,b
(2)连接仪器组装成如下图所示实验装置。某学生用抽拉法检查该装置的气密性,发现被拉出的注射器活塞一段时间后又回到原来的位置,你认为该装置是否漏气?。此处用分液漏斗代替长颈漏斗的优点是。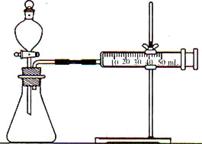
(3)实验室用高锰酸钾制取氧气,应选用的发生装置是(填字母),实验时该装置试管口应放一团棉花,其目的是;
该反应的文字表达式为。若用E装置收集产生的氧气,实验结束,停止加热前要先将导管移出水面,再熄灭酒精灯。这是为了防止
(4)若用过氧化氢溶液和二氧化锰制取氧气,则选用的发生装置是;该反应的文字表达式是;若用F装置收集产生的氧气,气体应从(填“c”或“d”)进入。
(5)装置G中的实验现象:红磷在氧气中剧烈燃烧,产生,该反应的表达式是。
(6)在标准状况下,空气的密度是1.29 g/L。某气体既能用D装置又能用E装置收集,则该气体可能是(填序号)
| 气体 |
A |
B |
C |
D |
| 标准状况下密度/(g .L-1) |
1.997 |
1.429 |
0.771 |
0.717 |
| 溶解性 |
可溶 |
微溶 |
易溶 |
难溶 |
(9分)化学是在分子、原子层次上研究物质性质、组成、结构与变化规律的科学。
(1)下列由美国《科学》杂志评出的2011年十大科学进展中的四项研究,主要属于化学探究领域的是
| A.研制出一种疟疾疫苗 | B.观测奇异的恒星系 |
| C.揭开人类起源之谜 | D.研究太空中的原始气体的组成 |
(2)某化学反应过程的微观示意图如下:
(图中“ ”和“
”和“ ”分别表示两种不同元素的原子)
”分别表示两种不同元素的原子)
①由上图还可以看出,分子是由构成的。
②上图中表示的物质属于纯净物的是(选填“反应前”或“反应后”)
③在化学反应前后,分子的种类(选填“一定改变”、“可能改变”或“一定不变”)
④化学变化中分子和原子的本质区别是。
(3)某同学对焊接切割金属的氧炔焰很感兴趣,他查阅资料后得知:
乙炔,化学符号为C2H2,俗电石气。在室温下是一种无色、极易燃的气体。纯乙炔在空气中燃烧火焰温度达2100度,在氧气中燃烧可达3600度。在烧焊金属方面有重要的用途。乙炔完全燃烧生成二氧化碳和水。
该同学根据所学化学知识决定设计实验验证乙炔燃烧的产物,进行了如下实验。
| 操作步骤 |
现象 |
结论 |
| 在氧气中点燃烧乙炔,在火焰上方罩一干燥而冷却的烧杯 |
出现水雾 |
乙炔燃烧有水生成 |
| 翻转烧杯,倒入,振荡 |
乙炔燃烧有二氧化碳生成 |
|
| 乙炔完全燃烧的表达式 |