[化学一选修2:化学与技术]
水是一种重要的自然资源,是人类赖以生存不可缺少的物质。水的处理主要包括水的净
化、污水处理、硬水软化和海水的淡化等。
(1)海水的淡化常用的方法有_________、_________、电渗析法等。
(2)电渗析法是近年来发展起来的一种较好的海水淡化技术,其原理如图所示。
①阳极(惰性电极)的电极反应式为 __________________.
②淡水的出口为a、b、c中的_________ 出口。
③某出口排出的浓海水中溴元素的含量为0.68g/L,现用氯气将其中的溴离子氧化为溴单质,则处理l.0×10 L该浓海水需标况下的氯气的体积为_________
L该浓海水需标况下的氯气的体积为_________ 。
。
(3) K2FeO4是自来水厂常用的消毒、净化剂。工业上常用Fe(NO3)3溶液与浓KCIO溶液在强碱性环境中生成K2FeO4,该反应的离子方程式为___________________________.
(4)氯碱工业常用_________(填“阴”或“阳”)离子交换膜电解槽电解精制的饱和食盐水, 若食盐水中含有杂质MgCl2则会对离子交换膜电解槽造成损害,其原因是_______ (用离子方程式表示)。
(5)工程塑料ABS合成时,用了以下三种单体: 、
、 ,请写出ABS的结构简式_______________________________。
,请写出ABS的结构简式_______________________________。
现有两种配合物晶体[Co(NH3)6]Cl3和[Co(NH3)5Cl]Cl2,请设计实验方案将这两种配合物区别开来。
实验方案:______________________________________________________________________
_______________________________________________________________________________。
根据下表中元素的电负性回答下列问题:
| 元素 |
Ca |
F |
S |
O |
C |
H |
P |
Cl |
Mg |
As |
| 电负性 |
1.0 |
4.0 |
2.5 |
3.5 |
2.5 |
2.1 |
2.1 |
3.0 |
1.2 |
2.0 |
有以下几种物质:CaF2、SO2、CH4、PCl3、MgO、AsH3、Cl2、HCl
(1)上述物质中的化学键为离子键的是______________________________。
(2)上述物质中的化学键为共价键的是______________________________。
(14分)氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,在将滤液按下图所示步骤进行操作。
回答下列问题:
(1)起始滤液的pH_____________7(填“大于”、“小于”或“等于”)原因是________________________________________。
(2)试剂I的化学式为______________________,①中发生反应的离子方程式为_________________________________________。
(3)试剂Ⅱ的化学式为______________________,②中加入试剂Ⅱ的目的是______________________________________;
(4)试剂Ⅲ的名称是______________________,③中发生反应的离子方程式为______________________________________;
(5)某同学称取提纯的产品0.7759g,溶解后定定容在100mL容量瓶中,每次取25.00mL溶液,用0.1000mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62mL,该产品的纯度为。
有A、B、C、D、E五种常见化合物,是由下列离子中的一种或几种形成的,阴离子有:硫酸根、硝酸根、碳酸氢根、氢氧根,阳离子有:钠离子、钾离子、铜离子、铝离子。
为了鉴别上述化合物。分别完成以下实验,其结果是:
①分别将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1) 写出B、D的化学式:B____________,D___________。
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为____________。
(3)在A溶液中加入少量澄清石灰水,其离子方程式为。
已知N2O4 (g) 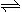 2NO2 (g)ΔH<0,
2NO2 (g)ΔH<0,
(1)现将1 mol N2O4 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是________。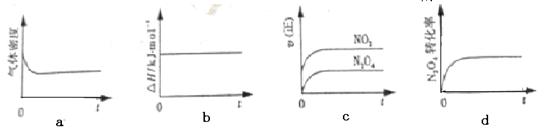
(2)若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数________(填“增大”、“不变”或“减小” )。反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________mol·L-1·S-1。
(3)NO2可用氨水吸收生成NH4NO3。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是(用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______(填”正向”“不”或“逆向”)移动。