已知H2A为弱酸,下列说法错误的是
A.0.1mol/L的Na2A溶液中:c(A2-)+c(HA-)+ c(H2A)= 0.1mol/L
B.常温下,将pH=3的H2A溶液稀释到原来的100倍,则稀释后溶液的pH<5
C.常温下,将pH=3的H2A溶液与pH=11的NaOH溶液等体积混合,反应混合液呈酸性
D.常温下,若1mol/L的NaHA溶液的pH=9,则溶液中:c(Na+)-c(HA-)-c(A2-)=10-5-10-9
2013年6月20日,中国成为世界上第二个成功进行“太空授课”的国家。如图为太空授课中航天员用注射器向水球内注入空气,在水球内产生了 两个标准的球形气泡,气泡既没有被挤出水球也没有融合到一起,水球也没有爆裂。下列说法错误的是
| A.实验是科学发现的重要手段,科学发现往往需要建立在实验事实的基础之上 |
| B.水的分子组成和结构,在太空中没有发生改变 |
| C.在太空实验中,如果往水球中分别注入氢气、氨气,同样也能观察到两个气泡 |
| D.水球实验中,可用吸水纸捕获洒落的水滴 |
用下图装置模拟人工肾脏的工作原理,电解生成的Cl2将尿素[CO(NH2)2]氧化成N2排出,则下列说法错误的是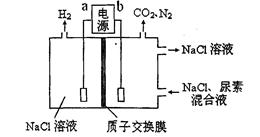
| A.电源的正极为b |
| B.尿素被氧化的化学方程式为CO(NH2)2+3Cl2+H2O=N2+CO2+6HCl |
| C.电解结束后,阴极室溶液与电解前相比pH增大 |
| D.阳极收集到气体4.48 L(标准状况)时,被氧化的尿素为6.0 g |
在密闭容器中进行反应M(g)+N(g)  Y(g)+2Z(?),产物Y在平衡混合物中的质量分数(Y%)不同温度、压强条件下随时间的变化如图所示,则下列叙述正确的是
Y(g)+2Z(?),产物Y在平衡混合物中的质量分数(Y%)不同温度、压强条件下随时间的变化如图所示,则下列叙述正确的是
| A.正反应为放热反应,Z是气体 |
| B.正反应为放热反应,Z是固体或液体 |
| C.正反应为吸热反应,Z是气体 |
| D.正反应为吸热反应,Z是固体或液体 |
四种短周期元素在元素周期表中的位置如右图所示,其中Z的原子半径最小。下列说法正确的是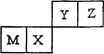
| A.M元素一定为金属元素 |
| B.X元素的最简单气态氢化物的热稳定性比Z元素的大 |
| C.若Y元素存在最高价含氧酸,其酸性比X元素的最高价含氧酸弱 |
| D.Z元素与氢元素一定能形成原子个数比为1︰1的共价化合物 |
下列说法正确的是
| A.将盐酸和醋酸钠溶液混合后溶液呈中性,溶液中c(Na+)=c(Cl-) |
| B.1 mol CH4分子中含有的共价键数目等于1 mol Na2O2固体中含有的离子总数 |
| C.80℃的纯水的pH大于25℃的纯水的pH |
| D.等体积、等物质的量浓度的NaCl溶液中离子总数大于NaClO溶液中离子总数 |