关于工业转化图(见下图),下列说法不正确的是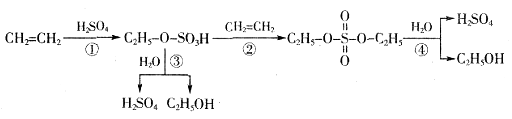
| A.该过程是一种“对环境友好型”工业生产硫酸的方法 |
| B.从以上物质的转化过程可看出硫酸可作乙烯水化法制乙醇的催化剂 |
| C.该过程中①②是加成反应 |
| D.该过程中③④是酯类的水解 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A.标准状况下,1mol H2O的体积约为22.4L |
| B.1 L 1mol/L Na2CO3溶液中Na+的物质的量为1mol |
| C.NA个氢气分子所占的体积为22.4L |
| D.常温常压下NA个二氧化碳分子的质量为44g |
在100mL的溶液中溶有0.1molNaCl和0.1molMgCl2,此溶液中Cl-的物质的量浓度为()
| A.3mol/L | B.2 mol/L | C.0.3 mol/L | D.0.2 mol/L |
下列有关0.1 mol/LNaOH溶液的叙述正确的是()
| A.该溶液中含有NaOH4g |
| B.100ml该溶液中含有Na+ 0.01mol |
| C.从1L该溶液中取出100mL,所取出的NaOH溶液的浓度为0.01 mol/L |
| D.在1L水中溶解4g NaOH即可配制得0.1 mol/L NaOH溶液 |
和22 g CO2所含分子数相等的水的质量为()
| A.44 g | B.22 g | C.18 g | D.9 g |
下列离子方程式与化学反应事实一致的是()
| A.硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-=Cu(OH)2↓ |
| B.石灰石溶于盐酸:CO32-+2H+=H2O+CO2↑ |
| C.硫酸溶液与氢氧化钾溶液反应:H++OH-=H2O |
| D.Cu和AgNO3溶液反应:Cu+Ag+=Cu2++Ag |