A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气球。关闭K2,将等量且少量的NO2通过K1、K3分别充入A、B中,反应起始时,A、B的体积相同。(已知:2NO2 N2O4△H<0)下列叙述正确的是
N2O4△H<0)下列叙述正确的是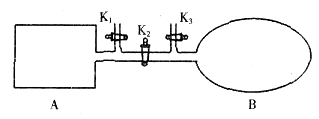
A. 到达平衡时A和B中NO2气体体积分数相同
B. 若在A、B中再充入与初始量相等的NO2,则达到平衡时A、B中NO2的转化率都增大
C. 若气球的体积不再改变,表明B中反应已达到平衡
D. 室温下,若设法使A、B都保持体积不变,将A套上一个绝热层,B与外界可以进行热传递,则达到平衡时B中气体的颜色较深
将4molA气体和2molB气体在2L的容器中混合,并在一定条件下发生反应:2A(g)+B(g)==2C(g).若经2s后测得C的浓度为0.6mol·L-1,下列几种说法,不正确的是()
①用物质A表示的平均反应速率为0.3mol·L-1·s-1②用物质B表示的平均反应速率为0.6mol·L-1·s-1③2s时物质A的转化率为70%④2s时物质B的浓度为0.7mol·L-1
| A.①③ | B.①④ | C.②③ | D.③④ |
硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产。下列对于反应 2SO2+O2
2SO2+O2 2SO3的说法中正确的是:()
2SO3的说法中正确的是:()
| A.只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B.该反应达到平衡后,反应就完全停止了,即正逆反应速率均为零 |
| C.在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |
| D.在达到平衡的体系中,充入由18O原子组成的O2后, 18O仅存在于SO2和SO3中 |
下列叙述中,甲金属一定比乙金属活泼性强的是:()
| A.甲原子电子层数比乙原子的电子层数多 |
| B.在甲乙两种金属和盐酸构成的原电池中,甲作正极,乙作负极 |
| C.1mol 甲和乙分别与足量的盐酸反应,产生H2的量:甲>乙 |
| D.常温时,甲能从水中置换出氢,而乙不能 |
下列关于元素周期表的叙述,正确的是:()
| A.ⅡA族中无非金属元素 | B.Ⅷ族中所含元素种类最多 |
| C.元素周期表中18个纵行对应18个族 | D.零族的所有元素均满足最外层电子数为8 |
某有机物含有C、H、O三种元素,其中氧的质量分数25%,相对分子质量小于150,一个分子中最多含C原子个数()
A、10 B、9 C、8 D、7