已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,A在反应中既不容易得电子也不容易失电子,元素B的最外层电子数是电子层数的3倍,元素D与A为同族元素,元素C和E形成的化合物CE是海水中的主要成分。下列说法不正确的是
A.离子半径:r(E)>r(B)>r(C)
B.熔点:CE>DE4
C.C与B形成的两种化合物中化学键类型不同
D.A、D、E的最高价氧化物对应水化物的酸性逐渐增强
用NA表示阿伏加德罗常数,下列说法中正确的是
| A.18g重水(2H216O)含有的电子数为10NA |
| B.3.4 g氨气分子中含有0.6NA个N—H键 |
| C.22.4L的NH3和16gCH4中所含有的电子数都是10NA |
| D.1molFeCl3完全转化为Fe(OH)3胶体后生成NA个胶粒 |
下图所示的实验方法、装置或操作完全正确的是
| A.除去CO2中的HCl | B.稀释浓H2SO4 |
| C.检查装置气密性 | D.研究不同催化剂对反应速率的影响 |
下列说法正确的是
| A.二氧化锰具有强氧化性,可用作H2O2分解的氧化剂 |
| B.二氧化硫和氯水均具有漂白性,两者混合使用将增强漂白效果 |
| C.在盛放食品的包装袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化变质 |
| D.锌与稀硫酸反应时加入几滴硫酸铜溶液可加快反应速率,原因是硫酸铜作催化剂 |
下列物质的分子中所含碳原子数相同(且不为1)时,其同类物质的同分异构体数目最多的是()
| A.烷烃 | B.饱和一元醇 | C.饱和一元醛 | D.饱和一元羧酸 |
化学工作者一直关注食品安全,发现有人将工业染料“苏丹红I号”非法用作食用色素,苏丹红是一系列人工合成染料,其中“苏丹红IV号”结构式如下: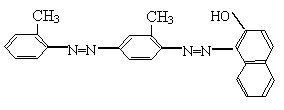
下列关于苏丹红Ⅳ的说法正确的是()
| A.不能发生加成反应 |
| B.分子中所有原子位于同一平面内 |
| C.可以使酸性高锰酸钾溶液褪色 |
| D.属于苯酚的同系物。 |