[化学—物质结构与性质]
Ⅰ.现今运动场馆大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED晶片,材质基本以GaAs(砷化镓)、InGaN(氮化铟镓)为主。砷化镓作为第三代半导体,以其为材料制造的灯泡寿命长,耗能少。
已知砷化镓的晶胞结构如图所示。请回答下列问题: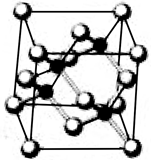
(1)下列说法正确的是 (填字母序号)。
a.砷化镓晶胞结构与NaCl相同 b.第一电离能:As>Ga
c.电负性:As>Ga d.砷化镓晶体中含有配位键
e.GaP与GaAs互为等电子体
(2)AsH3空间构型为__ __;砷化镓可由(CH3)3Ga 和AsH3在700℃时制得,(CH3)3Ga中镓原子的杂化方式为 。
Ⅱ. 金属铜的导电性仅次于银,居金属中的第二位,大量用于电气工业。
(3)Cu的价电子排布式为__________;请解释金属铜能导电的原因 。
(4)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中
含有的化学键除普通共价键外,还有 和 。已知NF3与NH3的空间构型都是三角锥形,单NF3不易与Cu2+形成配离子,其原因是 。
常温下,某溶液中由水电离出来的c(OH-)=1×10—11 mol/L,若向该溶液中滴入2—3滴酚酞,溶液的颜色可能是()
mol/L,若向该溶液中滴入2—3滴酚酞,溶液的颜色可能是()
| A.只显红色 | B.呈无色 | C.无色或粉红 | D.红色或无色 |
常温下,已知一种c(H+)=1×10-3 mol/L的酸和一种c(OH-)=1×10-3 mol/L的碱溶液等体积混合后溶液呈酸性,其原因可能是()
mol/L的酸和一种c(OH-)=1×10-3 mol/L的碱溶液等体积混合后溶液呈酸性,其原因可能是()
| A.浓的强酸和稀的强碱溶液反应有 | B.浓的弱酸和稀的强碱溶液反应 |
| C.等浓度的强酸和弱碱反应 | D.生成了一种强酸弱碱盐 |
在一定条件下,向密闭容器中充入30 mL CO和20 mL水蒸气,使其反应,当反应CO(g)+H2O(g) CO2(g)+H2(g)达到平衡时,水蒸气的体积分数与H2的体积分数相等,则下列叙述错误的是 ( )
CO2(g)+H2(g)达到平衡时,水蒸气的体积分数与H2的体积分数相等,则下列叙述错误的是 ( )
| A.平衡后CO的体积分数为40% | B.平衡后CO的转化率为25% |
| C.平衡后水的转化率为50% | D.平衡后混合气体的平均相对分子质量为24 |
如图表示反应M(g)+P(g) nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线
nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线 上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是 ( )
上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是 ( )
A.通过分析上图,该反应的正反应为放热反应
B.A状态与C状态的化学反应速率比较为v(A)<v(C)
C.在T1、D状态时,v正<v逆
D.在T2、B状态时,改变体积始终有v正=v逆,则n=2
已知中和热的数值是57.3KJ/mol。下列反应物混合时,产生的热量等于57.3KJ的是()
| A.1mol/L稀HCl(aq)和1mol/L稀NaOH(aq) |
| B.500mL2.0mol/L的HCl(aq)和500mL2.0mol/L的NaOH(aq) |
| C.500mL2.0mol/L的CH3COOH(aq)和500mL2.0mol/L的NaOH(aq) |
| D.1mol/L稀CH3COOH(aq)和1mol/L稀NaOH(aq) |