用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(l) △H=-574 kJ/mol
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ/mol
③H2O(g)=H2O(l) △H=-44kJ/mol。下列说法不正确的是
| A.等物质的量的CH4参加反应,反应①②转移的电子数相同 |
| B.CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-530 kJ/mol |
| C.0.2 mol CH4还原NO2至N2,且生成H2O(g)放出的热量为164.6 kJ |
| D.若用4.48 L(标准状况)CH4还原NO2至N2且生成H2O(g),整个过程中转移电子1.60 mol |
下列有关化学用语正确的是
A H2S的结构式:H—S—H BMg2+的结构示意图: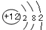
C二氧化碳的电子式: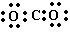 D考古时利用68C来测定一些文物的年代
D考古时利用68C来测定一些文物的年代
近年来,科学家正在探索利用铝粉作为新能源的可能性,以期铝能成为一种石油的取代物。假如铝作为一种普遍使用的新型能源被开发利用,关于其有利因素的下列说法,你认为哪项是错误的
| A.铝质轻,便于运输、贮存,且安全 |
| B.在地球上,铝矿资源比较丰富 |
| C.铝燃烧时放出的热量大,且燃烧后新产物对环境的污染容易得到有效的控制 |
| D.现代电解铝的工业技术已为铝作为新能源奠定了重要基础 |
3月28日,日本政府宣布从受到破坏的福岛第一核电站区域内土壤中检测出放射性钚-238( )、钚-239(
)、钚-239(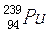 )和钚-240(
)和钚-240(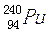 )。3月30日,在我国沿海和内地的部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素碘-131(
)。3月30日,在我国沿海和内地的部分地区空气中监测到来自日本核事故释放出的极微量人工放射性核素碘-131(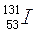 )。下列关于钚元素和碘元素的说法正确的是
)。下列关于钚元素和碘元素的说法正确的是
| A.钚-238、钚-239和钚-240是同素异形体的关系 |
| B.钚元素和碘元素在元素周期表中都属于主族元素 |
| C.碘-131原子的核外电子数是53,中子数是88 |
| D.基态碘原子的最外层电子排布式是5s25p5 |
下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
| A.通常情况下五种元素的单质中,Z单质的沸点最高 |
| B.Y、Z的阴离子电子层结构都与R原子的相同 |
| C.W的氢化物的沸点比X的氢化物的沸点高 |
| D.第一电离能:R>W>Y |
目前,科学界拟合成一种“二重构造”的球型分子,即把“足球型”的C60(富勒烯)溶进“足球型”的Si60分子中,外面的硅原子与里面的碳原子以共价键结合。下列关于这种分子的说法中正确的是
| A.是两种单质的混合物 | B.晶体属于原子晶体 |
| C.相对分子质量为2400 | D.分子中不含极性键 |