一定条件下存在反应:C(s)+H2O(g) CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
CO(g)+H2(g)△H>0。向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如下表,反应过程中CO的物质的量浓度随时间变化如图所示。
| 容器 |
甲 |
乙 |
丙 |
| 容积 |
0.5 L |
0.5 L |
V |
| 温度 |
T1 ℃ |
T2 ℃ |
T1 ℃ |
| 起始量 |
2 molC 1 molH2O |
1 molCO 1 molH2 |
4 molC 2 molH2O |
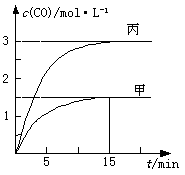
下列说法正确的是
A.甲容器中,反应在前15 min的平均速率v(H2)="0.1" mol·L-1·min-1
B.丙容器的体积V<0.5 L
C.当温度为T1 ℃时,反应的平衡常数K=2.25
D.乙容器中,若平衡时n(H2O)="0.4" mol,则T1< T2
500℃时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中H2、N2和NH3物质的量变化如右图所示,分析图像完成下列填空:
(1)0—10分钟,N2的平均反应速率为 ___________mol·L-1·min-1, 0—10分钟与10到20分钟两个时间段中,N2的反应速率之比为_________。反应在第10min可能改变的条件是____________,运用图像信息说明该条件不是升温的原因是____________。
(2)计算500℃时,反应N2+3H2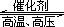 2NH3的平衡常数K的数值为_____________。保持温度不变,反应进行至25min时,抽去0.1mol氨,此时平衡常数K将_______(填“增大”或“减小”或“不变”)。保持体积不变,达到新平衡后的正反应的化学反应速率比原平衡状态_____(填“大”或“小”或“不变”)。
2NH3的平衡常数K的数值为_____________。保持温度不变,反应进行至25min时,抽去0.1mol氨,此时平衡常数K将_______(填“增大”或“减小”或“不变”)。保持体积不变,达到新平衡后的正反应的化学反应速率比原平衡状态_____(填“大”或“小”或“不变”)。
(3)在图中画出25min—40min时间段内N2的物质的量的变化图像。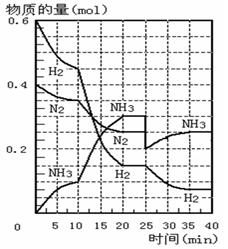
一定量的Zn与一定浓度的H2SO4反应,生成气体在标准状况下体积为2.24L。下列关于反应消耗的H2SO4的物质的量的推测肯定正确的是
| A.n(H2SO4)=0.1mol | B.n(H2SO4)=0.2mol |
| C.0.1mol<n(H2SO4) <0.2mol | D.0.1mol≤n(H2SO4)≤0.2mol |
如右图所示,X为铁、Y是石墨电极,a是饱和食盐水,实验开始前,在U形管的两边同时各滴入几滴酚酞试液,下列叙述错误的是
| A.合上K1、断开K2,该装置可以将化学能转变为电能 |
| B.合上K2、断开K1,一段时间后,湿润的KI淀粉试纸靠 近Y电极管口,试纸变蓝 |
| C.合上K1、断开K2,溶液中阴离子向Y电极定向移动 |
| D.合上K2、断开K1,一段时间后,X电极附近溶液呈红色 |
常温时,将V1mL c1 mol/L的氨水滴加到V2mL c2 mol/L的盐酸中,下列正确的是
| A.若混合溶液的pH=7,则溶液中c (NH4+)> c (Cl—) |
| B.若V1=V2,c1=c2,则溶液中一定存在c(H+)=c (OH—),呈中性 |
| C.若混合溶液的pH=7,则一定存在c1V1>c2V2 关系 |
| D.若V1=V2,并且混合液的pH<7,则一定是由于盐酸过量而造成的 |
脑白金主要成分的结构简式如下图所示,对脑白金主要成分的推论正确的是
| A.其分子式为C13H15N2O |
| B.该物质能发生水解反应并生成乙酸 |
| C.该物质不能与溴水反应 |
| D.其官能团与氨基酸相同 |