(15分)有机物A~H均含苯环,它们之间的转化关系如下。已知:B与FeCl3溶液混合无颜色变化。
回答下列问题:
(1)B的结构简式为 。
(2)①~⑦中属于取代反应的是 (填序号)。
(3)写出一种可鉴别D、F的试剂: 。
(4)写出反应⑦的化学方程式: 。
(5)写出同时符合下列条件的C的同分异构体的结构简式: 。
①化合物是1,3,5-三取代苯
②苯环上的三个取代基中分别含有醇羟基、酚羟基和醛
有机物A有下图所示转化关系。在A的质谱图中质荷比最大值为88,其分子中C、H、O三种元素的质量比为6∶1∶4,且A不能使Br2的CCl4溶液褪色;1 mol B反应生成了2 mol C。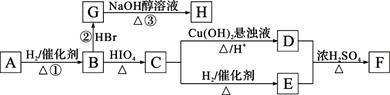
已知:RCH(OH)—CH(OH)R′ RCHO+R′CHO
RCHO+R′CHO
请回答下列问题:
(1)A的结构简式为_____________。
(2)若①、②、③三步反应的产率分别为90.0%、82.0%、75.0%,则由A合成H的总产率为_____________。
(3)D+E→F的反应类型为___________________。
(4)写出C与银氨溶液反应的离子方程式为______________________。
(5)若H分子中所有碳原子不在一条直线上,则H在一定条件下合成顺丁橡胶的化学方程式为__________。若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为________________。
(6)有机物A有很多同分异构体,请写出同时满足下列条件的一种异构体X的结构简式 。
a.X核磁共振氢谱有3个峰,峰面积之比为1∶1∶2
b.1 mol X可在HIO4加热的条件下反应,可形成1 mol 二元醛
c.1 mol X最多能与2 mol Na反应
d.X不与NaHCO3反应,也不与NaOH反应,也不与Br2发生加成反应
高聚酚酯是涂料行业中的新成员,其环保功能越来越受到人们的青睐。下图是某种高聚酚酯的合成路线图: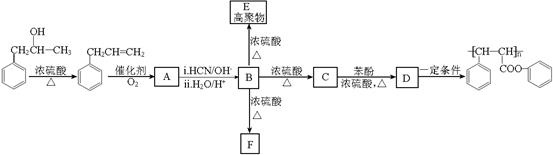
已知:①CH3CH==CH2 CH3CHO+HCHO;
CH3CHO+HCHO;
②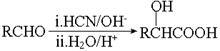 ;
;
③ F为含有三个六元环的酯。
请回答下列问题:
(1)A的化学名称为 ,B→F的反应类型是 。
(2)F的分子式为 ,E的结构简式为 。
(3)由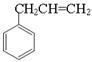 生成A的化学方程式为 。
生成A的化学方程式为 。
(4)C转化为D的化学方程式是 。
(5)B的同分异构体中,含有苯环、且苯环上有两个取代基、一个取代基中含有酯基、另一个取代基上含有醇羟基的有 种,其中核磁共振氢谱为5组峰,且峰面积之比为3:2:2:2:1的为 (任写一种结构简式)。
据下图的转化关系及现象回答下列问题。已知白色沉淀是碳酸钙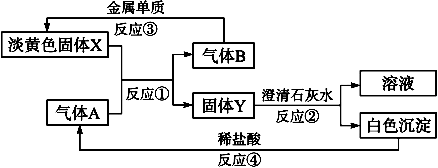
(1)固体X的名称______________;A的化学式______________。
(2)写出反应①②③④的化学方程式
①________________________________;
②________________________________;
③________________________________;
④________________________________。
下面是九种有机化合物的转化关系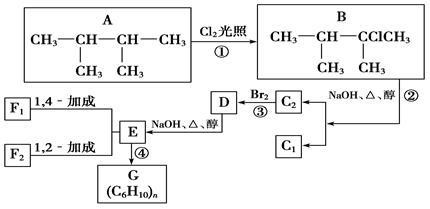
请回答下列问题:
(1)上述框图中,①是 反应,②是 反应,④是 反应。(填反应类型)
(2)化合物E是重要的工业原料,写出由D生成E的化学方程式:______________________。
(3)C2的结构简式__________;G的结构简式____________;F1和F2互为____________。
已知物质A~I之间的转化关系符合下图所示。其中A、C、F、G、I为常见固体且焰色反应均为黄色;A为海水中主要溶质,B为常温下常见液体;E为黄绿色气体,H是无色无味且能使澄清石灰水变浑浊的气体。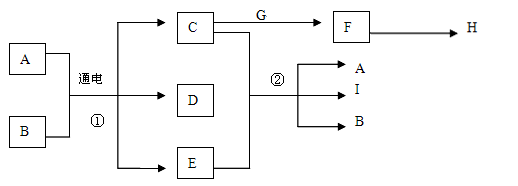
试回答下列问题:
(1)写出下列物质的化学式:D H
(2)反应①的化学方程式为: 。
(3)反应②的化学方程式为: 。