地球上总储水量很大,但淡水很少,海水中溶解了很多物质,又苦又咸,除了含H2O外,还含有大量的Na+ 、Ca2+、Cl-、Mg2+、SO42- 等。以海水为原料提取食盐的工艺流程如下: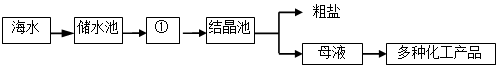
(1)图中①是 池(填“蒸发”或“冷却”)。
(2)根据海水晒盐的原理,下列说法中不正确的是 。
A. 得到的粗盐是纯净的氯化钠
B. 在①中,海水中水的质量逐渐减少
C. 在①中,海水中氯化钠的质量逐渐增加
D. 海水进入贮水池,海水的成分基本不变
(3)根据上述及工艺流程图,母液中所含的离子有 。
A. Ca2+、Mg2+、SO42-等 B. Na+ 、Ca2+、Cl-、Mg2+、SO42-、H2O等
C. Ca2+、Mg2+、SO42-、H2O等 D. Na+ 、Ca2+、Cl-、Mg2+、SO42-等
某化工厂的废液中,可能含有H2SO4.K2CO3.Na2SO4.KCl、FeCl3.HNO3六种物质中的两种。进行有关试验,所观察到的现象记录如下表。试根据各步实验及其现象进行分步推断,再推断所取的废液的可能组合。
| 步骤 |
实验操作 |
实验现象 |
推断(或结论) |
| (1) |
取废液放入试管观察 |
废液无色,澄清 |
废液中肯定不含FeCl3 |
| (2) |
用广泛pH试纸测定废液的pH |
测定结果:pH=3 |
|
| (3) |
向废液中滴入足量Ba(NO3)2溶液 |
有白色沉淀出现 |
|
| (4) |
向上述过滤所得的滤液中滴加AgNO3溶液 |
无明显反应现象 |
|
| 废液成分的可能组合(写出溶质的化学式) |
①_____________________ ②_____________________ ③_____________________ |
根据下列化合物与单质的相互转化关系(如下图)。请回答: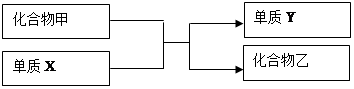
(1)若乙的溶液为浅绿色,Y是红色固体,则X是_______。
(2)在常温下若乙是气体,则X是______。
如图已知A、B、C、D、E、F为初中化学常见的物质,六种物质相互反应及转化关系如图: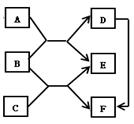
⑴若E为浅绿色溶液,D为无色气体,F为红色金属,则A的化学
式可能是 ,D可以与 反应生成F.
B、C反应方程式为 _______________________________.
⑵若B为能使澄清石灰水浑浊的无色气体, E通常为无色液体,则
F的化学式为 ,C能与 反应生成A.
A、B反应方程式为___________________________________
下图中的物质为初中化学所学的物质,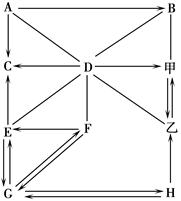
其中甲、乙属于常见单质,其余均为化合物。且B为黑色固体,E为难溶性固体,A、C、D、E为不同类别的物质。
请回答:
(1)写出E的化学式。
(2)G和H在组成上有何特点。
(3)写出下列反应的化学方程式
A→B ;
F→E 。
A~I都是初中化学中的常见物质,且有如图所示转化关系(部分反应物、生成物及反应条件均已略去)。已知A为金属单质,其它均为化合物。F为大理石的主要成分,E为一种常见的不挥发性酸。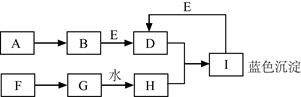
回答下列问题:
(1)写出下列物质的化学式:A Cu
、G。CaO
(2)写出反应的化学方程式:
①D溶液+H溶液:;②I+E溶液:。