固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的.它以固体氧化锆-氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过.该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应.下列判断正确的是 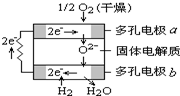
| A.有O2放电的a极为电池的负极 |
| B.a极对应的电极反应为:O2+ 2H2O+ 4e--= 4OH- |
| C.有H2放电的一极电极反应为:H2+O2- -2 e- =H2O |
| D.该电池的总反应方程式为:2H2+ O2= 2H2O |
N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g) 4NO2(g)+ O2(g) △H >0 T1温度下的部分实验数据为
4NO2(g)+ O2(g) △H >0 T1温度下的部分实验数据为
下列说法不正确的是
| A.500s内N2O5分解速率为2.96×10-3 mol/(L·s) |
| B.T1温度下的平衡常数为K1=125,1000s时转化率为50% |
| C.其他条件不变时,T2温度下反应到1000s时测得N2O5(g)浓度为2.98 mol/L,则T1<T2 |
| D.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1 >T2,则K1> K2 |
室温下,用0.100mol/L NaOH溶液分别滴定20.00ml 0.100mol/L 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是
| A.I表示的是滴定盐酸的曲线 |
| B.pH=7时,滴定醋酸消耗V(NaOH)小于20ml |
| C.V(NaOH) =20ml时,c(Cl—)==c(CH3COO—) |
| D.V(NaOH) =10ml时,醋酸溶液中:c(Na+ )>c(CH3COO—)>c(H+ )>c(OH—) |
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
| 选项 |
现象或事实 |
解释 |
| A |
用热的烧碱溶液洗去油污 |
Na2CO3可直接和油污反应 |
| B |
漂白粉在空气中久置变质 |
漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3 |
| C |
施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 |
K2CO3与NH4Cl反应生成氨气会降低肥效 |
| D |
FeCl3溶液可用于铜质印刷线路板制作 |
FeCl3能从含有Cu2+的溶液中置换出铜 |
下列实验操作或装置(略去部分加持仪器)正确的是
下列有关Fe2(SO4)3溶液的叙述正确的是
| A.该溶液中,K+、Fe2+、C6H5OH、Br—可以大量共存 |
| B.和KI溶液反应的离子方程式:Fe3++2I-=Fe2++I2 |
| C.和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓ |
| D.1L0.1mol/L该溶液和足量的Zn充分反应,生成11.2gFe |