设阿伏加德罗常数的值为NA,则下列说法正确的是
| A.标准状况下,11.2L CCl4所含的分子数为0.5NA |
| B.常温常压下,4.2g C2H4和C8H16的混合物中含有的碳原子数为0.3NA |
| C.7.8g苯分子中碳碳双键的数目为0.3 NA |
| D.6.4gCu与20mL10 mol·L-1浓硫酸反应,转移的电子数为0.2NA |
下列实验装置不能达到实验目的的是()
氯酸是一种强酸,浓度超过40%时会发生分解,反应可表示为:a HClO3 = bO2↑+ c Cl2↑+ d HClO4 + e H2O。用湿润的淀粉碘化钾试纸检验气体时,试纸先变蓝后褪色。下列有关说法正确的是()
| A.由反应可确定:氧化性HClO4>HClO3 |
| B.该反应的还原产物是O2和HClO4 |
| C.试纸先变蓝后褪色是因为Cl2具漂白性 |
| D.若化学计量数a=8,b=3,则该反应转移电子数为20e- |
将等物质的量的金属Na、Mg、Al分别与100 mL 2 mol/L的盐酸反应,实验测得生成气体的体积V(已折合为标准状况)与时间t的关系如下图所示,则下列说法错误的是()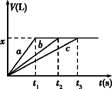
| A.x=2.24 |
| B.钠的物质的量为0.2 mol |
| C.反应时,Na、Mg、Al均过量 |
| D.曲线b为Mg与盐酸反应的图像 |
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是()
| A.原子半径由小到大的顺序为Y<Z<X<W |
| B.X的简单氢化物的热稳定性比W的强 |
| C.化合物YX、ZX2、WX3,中化学键的类型相同 |
| D.W的最高价氧化物对应水化物的酸性比Z的弱 |
常温下,下列各组离子在指定溶液中一定能大量共存的是()
| A.水电离的c( H+)= 1xl0-13 mol/L的溶液中:K+、Na+、SiO32-、SO42- |
| B.能使石蕊呈蓝色的溶液中:Na+、Fe3+、SO42-、Cl- |
C.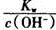 =lxl0-13 moI/L的溶液中:Ba2+、ClO-、Cl-、NO3- =lxl0-13 moI/L的溶液中:Ba2+、ClO-、Cl-、NO3- |
| D.能与铝反应放出H2的溶液中:Fe2+、K+、SO42-、Cl- |