|
为了配制100 mL 1 mol·L-1的NaOH溶液,其中有下列几个操作:①NaOH固体放在纸上进行称量 ②选刚用蒸馏水洗净的100 mL容量瓶进行配制 ③NaOH在烧杯里刚好完全溶解,立即把溶液转移到容量瓶中 ④用蒸馏水洗涤烧杯内壁2次,洗涤液也均转入容量瓶中 ⑤使蒸馏水沿玻璃棒注入容量瓶,直到溶液的凹液面恰好与刻度线相切。其中操作错误的是
A.①②③ B.③④⑤关于O2与O3气体,下列比值一定为2:3的是()
| A.若两种气体所占体积相同,两种气体的质量之比 |
| B.若温度及压强相同,两种气体的密度之比 |
| C.若两种气体原子数相同,两种气体的质子数之比 |
| D.若两种气体的质量相同,两种气体的分子数之比 |
下图图一是硫酸试剂标签上的部分内容。下列说法正确的是()
| A.该硫酸的物质的量浓度为9.2 mol/L |
| B.该浓硫酸中溶质、溶剂分子数目之比为9:1 |
| C.在盛放该药品的标签上应标出如图二所示的警示标记 |
| D.该硫酸与等质量的水混合所得溶液的物质的量浓度等于9.2 mol/L |
为确定某溶液的离子组成,进行如下实验:
①实验测定溶液显强碱性。②取少量溶液加入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体。③在②所得溶液中再滴加Ba(NO3)2溶液,无白色沉淀,再滴加AgNO3溶液,产生白色沉淀。以下推测正确的是()
| A.一定有SO42— | B.一定有Cl- |
C.一定有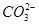 |
D.不能确定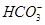 离子是否存在 离子是否存在 |
下列叙述中不正确的是( )
| A.电解质是指在熔融状态和水溶液中均能导电的化合物 |
B.同温同压下,任何不同气体分子的间距均几乎相同 |
C.复分解反应一定不是氧化还原反应 |
D.1molAl与盐酸或氢氧化钠溶液完全反应时,失去电子数目均为3NA |
现有三组实验:①除去混在植物油中的水 ②用CCl4回收碘水中的碘 ③海水的淡化,分离以上各混合液的正确方法依次是()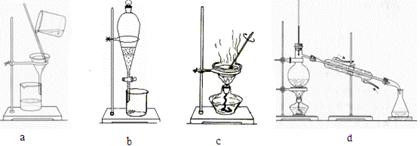
| A.d、 bc、 d | B.b、 bd、 d | C.b、 bc、 c | D.d、 bd、 c |