某温度下,体积一定的密闭容器中进行如下可逆反应:X(g)+Y(g) Z(g)+W(s);ΔH>0。下列叙述正确的是
Z(g)+W(s);ΔH>0。下列叙述正确的是
| A.加入少量W,逆反应速率增大 | B.升高温度,平衡逆向移动 |
| C.平衡后加入X,上述反应的ΔH增大 | D.当容器中气体压强不变时,反应达到平衡 |
设NA为阿伏伽德罗常数的数值。下列说法正确的是
| A.0.1 mol·L-1的NaF溶液中所含F-的数目小于0.1NA |
| B.标准状况下,2.24L乙醇中含有的C—H键数目为0.5NA |
| C.0.1 molNa完全被氧化生成Na2O2,转移电子的数目为0.1NA |
| D.0.1 molO3和O2的混合气体中含氧原子数目为0.2NA |
除去下列括号内杂质的试剂或方法错误的是
| A.N2(O2):通过灼热的镁粉 |
| B.SiO2(Fe2O3):足量的盐酸,过滤 |
| C.CO2(SO2):酸性KMnO4溶液、浓硫酸,洗气 |
| D.C2H5OH(CH3COOH):加足量CaO,蒸馏 |
下列实验装置或操作设计正确且能达到实验目的的是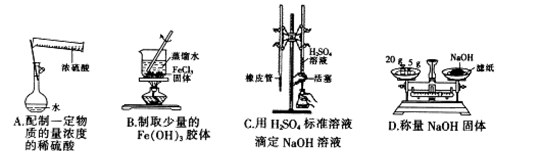
“富勒烯”家族又增添了新成员,继C60、C70、N60之后,中美科学家首次发现了全硼富勒烯B40.下列说法正确的是
| A.B40、C70都属于新型化合物 | B.C60和14C互称同位素 |
| C.B40、C60、C70、N60都属于烯烃 | D.B40、C60、C70、N60都只含共价键 |
下列说法正确的是
| A.硫酸、纯碱、醋酸钠和生石灰分别属于酸、碱、盐和氧化物 |
| B.蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C.Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 |
| D.日常生活中无水乙醇常用于杀菌消毒 |