化合物A、B是中学常见的物质,其阴阳离子可从下表中选择
(1)若A、B的水溶液均为无色,B的水溶液呈碱性,且混合后只产生不溶于稀硝酸的白色沉淀及能使红色石蕊试纸变蓝的气体。
①A的化学式为____ ;B的化学式为____;
②A、B溶液混合后加热量中性反应的离子方程式为 。
(2)若A的水溶液呈浅绿色,B的水溶液呈无色且其焰色反应为黄色。向A的水溶液中加入稀盐酸无明显现象,再加入B后溶液变黄,但A、B的水溶液混合亦无明显变化。则
①A为____ ;B为 ;
②经分析上述过程中溶液变黄的原因可能是有两种:
I ;相关的离子反应方程式 。
II ;相关的离子反应方程式 。
(10分)某化学研究性小组在用铝与稀硫酸的反应制氢气的实验时发现,如果把在空气中放置一段时间的5.0 g铝片放入圆底烧瓶中,然后通过分液漏斗加入500 mL 0.5 mol/L硫酸溶液,充分反应后,该小组同学根据记录数据得到了产生氢气的速率与反应时间的关系图象(如图所示) ,请你帮助该小组同学回答下列问题: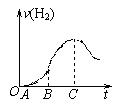
(1)曲线OA段不产生氢气的原因是_____________ _ ______
____________________ _____,
有关的离子反应方程式为______________________________ _____
(2)曲线BC段产生氢气的速率突然加快的主要原因是
____________________________________________________________________________
(3)点C以后产生氢气的速率逐渐减小的主要原因是
____________________________________________________________________________
(4)从理论上分析该小组同学能收集到氢气的体积为(标准状况下)___________
某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是。
(2)根据上述框图反应关系,写出下列B、C、D、E所含物质的化学式
固体B;沉淀C;沉淀D;溶液E。
(3)写出①、②、③、④四个反应方程式(②、③写离子方程式①、④写化学方程式)
①;②;
③;④。
下表标出的是元素周期表的一部分元素,回答下列问题:
| 1 |
||||||||||||||||||
| 2 |
D |
B |
A |
|||||||||||||||
| 3 |
J |
I |
H |
C |
G |
F |
E |
|||||||||||
| 4 |
L |
K |
N |
|||||||||||||||
| 5 |
M |
|||||||||||||||||
| 6 |
(1)表中用字母标出的14种元素中,化学性质最不活泼的是(用元素符号表示,下同),非金属性最强的是,常温下单质为液态的非金属元素是.J、C、F中,原子半径最小的元素是;属于过渡元素的是(该空用字母表示),第六周期的元素共有种。
(2)F,C气态氢化物中其中以(填化学式)最不稳定;第三周期对应的碱性最强的最高价氧化物的水化物的化学式是,该物质含有的化学键类型是,用该物质做焰色反应实验,火焰呈色。
(3)N元素在周期表中的位置是,写出由F单质制取N单质的离子方程式是。
生活中的一些问题常涉及化学知识,下列叙述不正确的是(填序号)
。
①淀粉、蛋白质都是天然有机高分子化合物
②食用植物油的重要成分是高级不饱和脂肪酸甘油酯,是人体的营养物质
③禁止使用含铅汽油是为了提高汽油的燃烧效率
④洗涤剂去污是物理变化,碱液去污属于化学变化
⑤随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了防止中秋月饼等富脂食品氧化变质,延长食品的保质期,在包装袋中常放入生石灰
⑥现在用的清洁燃料主要有两类:一类是压缩天然气,另一类为液化石油气,他们都属于碳氢化合物
⑦福尔马林是一种良好的杀毒剂,也可用来消毒自来水
⑧为保证加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉
硝酸工业在国民经济、国防工业和航天事业中占有重要地位。随着化学纤维、近代有机合成、火箭、导弹等工业的迅速发展,需要使用大量的硝酸。
(1)工业生产中用铂系金属作为催化剂,用氨氧化法制取硝酸。写出用铂铑合金作催化剂由氨氧化制备硝酸的第一步反应的化学方程式 ▲。浓硝酸和浓硫酸的混合酸是有机合成中常用的硝化剂,写出将苯滴入浓硝酸和浓硫酸混合液中,并在50℃--60℃反应的化学方程式 ▲。
(2)铜既能与稀硝酸反应,也能与浓硝酸反应,当铜与一定浓度硝酸反应时,可将方程式表示为:Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O (方程式未配平)。则硝酸在该反应中的作用是 ▲。如果得到的NO和NO2物质的量相同,写出并配平该反应的离子方程式 ▲,0.6mol Cu被硝酸完全溶解后,若用排水法收集这些气体,可得标准状况下的气体体积为 ▲。