(7分)实验课上,小舟同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
(1)小帆同学却说:“这种无色溶液中不一定含有氢氧化钠”他做了如下实验
| 实验步骤 |
实验现象 |
实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 |
无色酚酞试液变红 |
无色溶液中含有氢氧化钠 |
小玉认为小帆的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是:
。
(2)小玉设计了另一个实验:
| 实验步骤 |
实验现象 |
实验结论 |
| ①取少量样品于试管中,加入 ②过滤,向滤液中滴加几滴硫酸铜溶液 |
③ ④ |
无色溶液中确实含有氢氧化钠 |
小玉的实验可靠性高的原因是① 。
② 。
某校兴趣小组对氢氧化钠溶液与稀盐酸混合后的有关问题,进行了如下探究,请同学们一起参与此次探究之旅.
(1)探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全中和?
[方案设计]小亮、小丽、小林三位同学设计了如下方案进行探究:
| 方案设计者 |
方案步骤 |
方案预估现象 |
方案预估结论 |
| 小亮 |
取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞溶液,振荡 |
酚酞溶液不变色 |
恰好完全中和 |
| 小丽 |
用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,把试纸呈现的颜色与标准比色卡对照 |
pH=7 |
恰好完全中和 |
| 小林 |
取少量反应后的溶液于一支试管中,并向试管中滴加稀硝酸和硝酸银溶液 |
有白色沉淀生成 |
盐酸过量,没有完全中和 |
[方案评价]请判断以上设计的三个方案中,____① ____同学的方案是正确的.
[方案反思]请分析另外两个方案错误的原因:____②____;____③____.
(2)探究二:氢氧化钠溶液与稀盐酸混合后,所得溶液中溶质的成分是什么?
[作出猜想]小亮猜想:溶质有NaCl、HCl、NaOH;
小丽猜想:溶质只有NaCl;
小林猜想:溶质有NaCl、HCl;
你的猜想:溶质有____①____(填化学式).
小丽认为小亮的猜想是错误是,她的理由是____②____.
[实验设计及验证]请你将下列报告填写完整:
| 实验操作 |
实验现象 |
实验结论 |
| 取反应后的溶液于试管中,加入碳 酸钠溶液 |
③ |
小林猜想正确 |
| ④ |
有蓝色沉淀生成 |
你的猜想正确 |
小明向氢氧化钠溶液中滴加稀盐酸,发现没有明显现象.为了判断两者是否恰好完全反应,他取少量反应后的溶液加入试管中,滴加几滴无色酚酞试液,振荡后观察到酚酞试液不变色.
(1)根据上述现象,小明得出“两种物质恰好完全反应”的结论.小白认为小明的结论是不合理的,其理由是________.
(2)小白利用pH试纸测反应后溶液的pH,以确定两者是否恰好完全反应.请你选用其他试剂再设计一个实验,以验证氢氧化钠和盐酸是否恰好完全反应(要求写出选用的试剂、可能观察到的现象和相应的结论)________.
(3)小白为了继续探究“在氢氧化钠与盐酸反应的过程中,溶液的pH是如何变化的”这一问题,进行如下实验:在一定量的氢氧化钠溶液中逐渐滴加盐酸,用pH试纸测定溶液的pH,记录数据如下表:
| 盐酸的体体/mL |
0 |
10 |
19.5 |
20 |
20.5 |
30 |
40 |
| pH |
13 |
12 |
10 |
7 |
3 |
2 |
1 |
下图中能合理表示该反应过程中溶液pH变化的是________.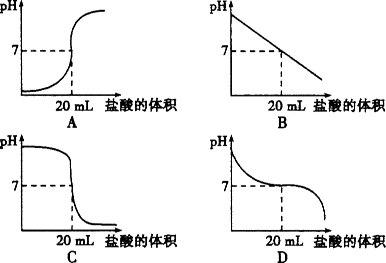
在研究酸和碱的化学性质时,某小组同学想证明:稀硫酸与氢氧化钠溶液混合后,虽然仍为无色溶液,但确实发生了化学反应,请与他们一起完成实验方案的设计、实施和评价。
(1)方案一:测定稀硫酸与氢氧化钠溶液混合前后的pH(20℃).
测定某氢氧化钠溶液的pH,pH______(填“大于”“等于”或“小于”)7.
将一定量的稀硫酸加入该氢氧化钠溶液中,混合均匀后测定其pH,pH小于7.
结论:稀硫酸与氢氧化钠溶液发生了反应,并且_____过量。
(2)方案二:观察________________________________.(根据图所示实验步骤,概括方案要点)。
结论:稀硫酸与氢氧化钠溶液发生了化学反应,反应的化学方程式为__________________.
(3)上述两个方案在设计思想上的相同点是________________________________________.
(4)为了进一步获取稀硫酸与氢氧化钠溶液确实发生了化学反应的证据,依据中和反应是_________(填“放热”“吸热”或“无热量变化”)反应,采用同温下的稀硫酸与氢氧化钠溶液进行实验,整个实验中至少需要测定溶液温度___________次。
盐酸中含有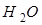 分子、
分子、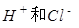 离子,要探究是哪一种粒子能使紫色石蕊溶液变成红色,请观察在白色点滴板上进行的下列实验,将实验现象和结论填入下表。
离子,要探究是哪一种粒子能使紫色石蕊溶液变成红色,请观察在白色点滴板上进行的下列实验,将实验现象和结论填入下表。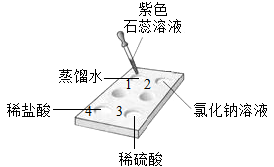
| 滴加紫色石蕊溶液后的现象 |
结论 |
|
| 第1孔 |
孔中溶液仍为紫色 |
水分子________ |
| 第2孔 |
||
| 第3孔 第4孔 |
二氧化硫是造成酸雨的主要物质之一。小丽为探究二氧化硫能与水反应生成酸,设计了如下实验方案。
【实验设计】她先用紫色石蕊溶液将白色滤纸浸润,干燥后做成紫色的小花,然后按下列图示进行实验。观察到实验(I)和(III)中的小花变红,(II)中的小花不变色。
【评价反思】小虎对小丽的实验方案提出了质疑,他认为上述实验不足以证明“二氧化硫和水反应生成了酸”。两位同学仔细讨论后认为还需补充如下一个实验,才能得出二氧化硫与水反应生成酸。
| 实验操作 |
实验现象 |
| __________________ |
__________________ |
【拓展应用】二氧化硫也是实验室一种污染气体,常用碱液吸收。写出实验室用氢氧化钠溶液吸收二氧化硫的化学方程式:_____________________________________________.