矿石中金的含量很低,金的性质又相当稳定,只能用湿法冶金——氰化法提炼,即采用稀的NaCN溶液处理已粉碎的矿石,把少量的金浸入溶液中,然后用金属锌作还原剂将金从溶液中置换析出。其反应原理为
①4Au+8NaCN+O2+2H2O 4Na[Au(CN)2]+4NaOH;
4Na[Au(CN)2]+4NaOH;
②2Na[Au(CN)2]+Zn 2Au+Na2[Zn(CN)4]。
2Au+Na2[Zn(CN)4]。
以下有关氰化法提炼金的说法中正确的是
| A.Na[Au(CN)2]不溶于水 |
| B.化合物Na[Au(CN)2]中金元素的化合价为+1 |
| C.金元素在地壳中能以化合态的形式存在 |
| D.在提炼过程中含金元素的物质始终作氧化剂 |
下列图示与对应的叙述不相符的是()
| A.图1表示相同温度下,向pH=10的氢氧化钠溶液和氨水中分别加水稀释时pH的变化曲线,其中a表示氨水稀释时pH的变化曲线 |
| B.图2表示向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸所得沉淀物质的量与盐酸体积的关系 |
C.图3表示压强对可逆反应CO(g)+H2O(g)  CO2(g)+H2(g)的影响,乙的压强比甲的压强大 CO2(g)+H2(g)的影响,乙的压强比甲的压强大 |
| D.图4表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量的0.1 mol·L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化(Mn2+对该反应有催化作用) |
下列离子方程式正确的是()
| A.向AlCl3溶液中滴加氨水:Al3++3OH-=Al(OH)3↓ |
| B.向NaHCO3溶液中加入少量Ca(OH)2溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
C.向苯酚溶液中滴加Na2CO3溶液: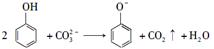 |
| D.向氯化亚铁溶液中滴加稀硝酸:3Fe2++4H++ NO3-=3Fe3++NO↑+2H2O |
下列物质转化在给定条件下不能实现的是()
①Si SiO2
SiO2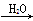 H2SiO3;②S
H2SiO3;②S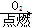 SO3
SO3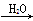 H2SO4;③C
H2SO4;③C CO2
CO2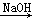 Na2CO3
Na2CO3
④MgCl2溶液 MgCl2·6H2O
MgCl2·6H2O Mg;⑤Na
Mg;⑤Na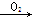 Na2O2
Na2O2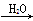 NaOH
NaOH
| A.①②③ | B.①②④ | C.①②③④ | D.①②③④⑤ |
设NA为阿伏加德罗常数的值。下列说法一定正确的是()
| A.9.2 g C7H8和C3H8O3的混合物中所含氢原子总数为0.8NA |
| B.标准状况下,11.2 L C2H5OH中所含的分子数为0.5NA |
| C.将含0.1 mol FeCl3的溶液滴加到沸水中完全水解可生成0.1NA个Fe(OH)3胶粒 |
| D.0.1 mol Na2O2参加反应转移的电子数目是0.2NA |
下列有关物质的性质与应用相对应的是()
| A.氢氟酸具有弱酸性,可用于雕刻玻璃 |
| B.Na2O2具有强氧化性,可用作自来水的消毒剂 |
| C.氯化铁溶液能氧化铜单质,可用于制作印刷电路板 |
| D.SO2具有漂白性,可使酸性高锰酸钾溶液褪色 |