工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2  2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法错误的是
2SO3,这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法错误的是
| A.使用催化剂是为了加快反应速率,提高生产效率 |
| B.在上述条件下,SO2不可能100%地转化为SO3 |
| C.为了提高SO2的转化率,应适当提高O2的浓度 |
| D.达到平衡时,SO2的浓度与SO3的浓度相等 |
日常生活中的许多现象都与化学反应有关,下列现象与氧化还原反应无关的是()。
| A.铁制菜刀生锈 |
| B.酸雨腐蚀大理石雕像 |
| C.铜制饰品上出现绿色斑点[Cu2(OH)2CO3] |
| D.铝锅表面生成致密的氧化膜 |
已知,粗盐中除了含有少量的泥沙外,还含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,先将粗盐溶于水后,再通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液; ③加入稍过量的BaCl2 溶液;④滴入稀盐酸至溶液呈中性;⑤过滤。正确的操作顺序是
| A.②①③⑤④ | B.⑤③②①⑤④ | C.⑤②③①④⑤ | D.③⑤②①④ |
下列反应的离子方程式书写正确的是()
| A.向澄清石灰水中滴入盐酸:Ca(OH)2+2H+===Ca2++2H2O |
| B.用小苏打治疗胃酸过多:HCO3-+H+===CO2↑+H2O |
| C.实验室用石灰石和盐酸反应制取CO2:CO32-+2H+===CO2↑+H2O |
| D.Ba(OH)2与H2SO4反应:H++OH-===H2O |
Na与水反应的化学方程式2Na + 2H2O ="=" 2NaOH + H2↑,在反应中水()
| A.是氧化剂 | B.是还原剂 |
| C.既是氧化剂又是还原剂 | D.既不是氧化剂又不是还原剂 |
实验室有三瓶失去标签的试剂,分别是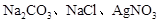 ,实验员选择了一种试剂就把它们区别开来了,这种试剂是()
,实验员选择了一种试剂就把它们区别开来了,这种试剂是()
| A.盐酸 | B.氢氧化钠溶液 | C.氯化钡溶液 | D.硝酸 |