已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,其中X原子最外层电子数是其电子层数的2倍。下列说法正确的是
| A.四种元素的原子半径大小rY>rW>rX>rZ |
| B.元素X的含氧酸只有一种,元素Y则有两种 |
| C.元素Z的气态氢化物的稳定性比元素Y的强 |
| D.元素Y和W的氧化物是导致酸雨的主要原因 |
目前,人类已经发现的非金属元素除稀有气体元素外共有16种,下列对这16种非金属元素的判断不正确的是
①都是主族元素,原子的最外层电子数都大于3
②单质在反应中都只能作氧化剂
③对应的含氧酸都是强酸
④氢化物常温下都是气态,所以又叫气态氢化物
⑤气态氧化物与水反应都不会再生成气体
| A.全部 | B.只有①② | C.只有①②③④ | D.只有①②④⑤ |
下列关于金属元素特征的叙述正确的是
①金属元素的原子只有还原性,离子只有氧化性;
②金属元素在化合物中一般显正价;
③金属性越强的元素相应的离子氧化性一般越弱;
④金属元素只有金属性,没有非金属性;
⑤最外层电子数越多的金属原子,金属性越强;
⑥离子化合物一定含金属元素。
| A.①②③ | B.②③ | C.①⑤⑥ | D.全部 |
M、N都是短周期元素,原子半径M>N,它们可形成化合物MN2,由此得出的正确判断是
| A.M、N不可能在同一周期 | B.M一定在N的下一周期 |
| C.MN2肯定是共价化合物 | D.M、N可能在同一主族 |
如果把Cu、Zn与稀H2SO4构成的原电池表示为 ,则下列能表示原电池的是
,则下列能表示原电池的是
A.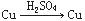 |
B.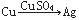 |
C.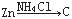 |
D. |
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列“水”电池在海水中放电时的有关说法正确的是
| A.正极反应式:Ag+Cl﹣﹣e﹣=AgCl |
| B.每生成1mol Na2Mn5O10转移2mol电子 |
| C.Na+不断向“水”电池的负极移动 |
| D.AgCl是还原产物 |