常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.1.0 mol/L的NaHSO4溶液:K+、Fe2+、NO3-、Cl- |
| B.l.0 mol·L-1 NaClO溶液:Fe2+、K+、I一、Cl- |
| C.甲基橙显黄色的溶液: Na+、CO32-、NO3-、SO32- |
| D.在c(H+)/c(OH-) = 1×1013的溶液:NH4+、Ca2+、C1-、K+ |
用NA表示阿伏加德罗常数,以下各说法中不正确的是
| A.1mol钠作为还原剂可提供的电子数为NA |
| B.17g NH3中所含电子个数为10 NA |
| C.22.4LN2分子中所含原子数为2 NA |
| D.1L2mol·L-1的Mg(NO3)2溶液中含NO3-个数为4 NA |
科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是
| A.原子数 | B.分子数 | C.体积 | D.物质的量 |
在不用指示剂的前提下,欲将含有盐酸的氯化钙溶液中的盐酸除去,最好选用下列物质中的
| A.碳酸钙 | B.石灰水 |
| C.氢氧化钠 | D.熟石灰 |
具备基本的化学实验技能是进行科学探究的基础和保证。下列有关实验操作正确的是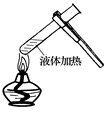
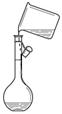
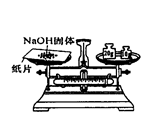
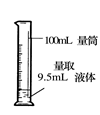
| A.给液体加热 | B.转移溶液 | C.称取NaOH固体 | D.量取液体 |
盛有一向定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似的用下图中的曲线表示是