甲、乙两种固体的溶解度曲线如图所示。下列说法中,正确的是
| A.20℃时,甲、乙溶液中溶质的质量一定相等 |
| B.40℃时,分别在100 g水中加入45 g甲、乙, 所得甲、乙溶液的溶质的质量分数相等 |
| C.40℃时,将10%的甲溶液降温至20℃,溶液中溶质的质量分数不变 |
| D.40℃时,将甲、乙的饱和溶液降温至20℃,析出晶体的质量甲大于乙 |
如图所示,图中 和
和 分别表示两种不同质子数的原子,其中表示单质的是
分别表示两种不同质子数的原子,其中表示单质的是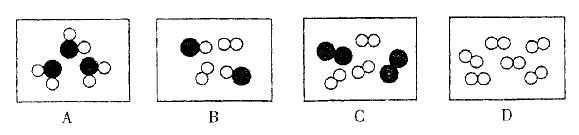
下列符号中既能表示一种元素,又能表示该元素的一个原子,还能表示一种物质的是
| A.H | B.Fe | C.O2 | D.CO2 |
新型净水剂铁酸钠(Na2FeO4)中,铁元素的化合价是
| A.+5 | B.+3 | C.+2 | D.+6 |
苏州博物馆最近启用新购置的“真空充氮杀虫灭菌消毒机”来处理和保护文物.即将文物置于该机器内,三天后氮气浓度可达99.99%;再密闭三天左右,好氧菌、厌氧菌和丝状霉菌都被杀灭。下列有关氮气说法错误的是
| A.通常状况下氮气易溶于水 |
| B.氮气不能供给呼吸 |
| C.通常情况下氮气的化学性质不活泼 |
| D.高浓度氮气可抑制菌类的生长 |
钠元素和氯元素的本质区别是
| A.原子最外层电子数不同 | B.原子的质子数不同 |
| C.原子的电子层数不同 | D.原子的中子数不同 |