学过金属活动性后,秦思同学通过实验探究锌粉与硝酸亚铁和硝酸银两种盐溶液的反应。实验现象和数据如下: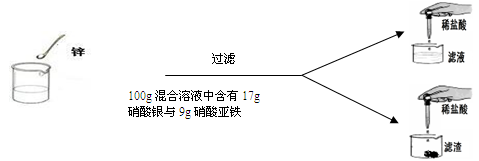
| |
第一次 |
第二次 |
第三次 |
第四次 |
| 硝酸亚铁与硝酸银的混合溶液 |
100g |
100g |
100g |
100g |
| 锌粉 |
2g |
3.25g |
m |
9.75g |
| 向滤液中加入稀盐酸后的实验现象 |
产生白色沉淀 |
无明显现象 |
无明显现象 |
无明显现象 |
| 向滤渣中加入100 g稀盐酸后的实验现象 |
无明显现象 |
无明显现象 |
产生气泡,溶液变为浅绿色 |
现象与第三次相同 |
(1)第四次向滤渣中加入稀盐酸后产生气泡的化学方程式为 ;
(2)根据第一次的实验现象,你认为此次滤液中的溶质是 ;
(3)根据已知条件列出求解第二次实验中置换出金属银的质量(x)的比例式 ;
(4)若第三次实验锌与两种盐溶液恰好完全反应,则m的质量为__________________;
(5)若向第三次反应后的滤液中加入一定质量的水,所得不饱和溶液中溶质的质量分数为10%,则加入水的质量为__________________;
(6)若用溶质质量分数为36.5%的浓盐酸配制第四次实验中与滤渣恰好完全反应所需的稀盐酸,则需要浓盐酸与水的质量比为_______________。
10g镁与足量稀硫酸反应,生成氢气多少克?
(反应的化学方程式为:Mg + H2SO4 ="=" MgSO4 + H2↑)
80g石灰石样品与足量稀盐酸完全反应后(样品中的杂质既难溶于水,又不与稀盐酸反应),将反应容器内的物质过滤后称得的固体物质质量为20g。(固体上残留的液体质量忽略不计)计算:
(1)该石灰石样品可制取二氧化碳的质量。
(2)该石灰石样品中碳酸钙的质量分数是多少?
乙炔(C2H2)是一种重要的化工原料,实验室常用碳化钙(CaC2)与水反应制取乙炔,该反应方程式为:CaC2 + 2H2O →Ca(OH)2 + C2H2↑。计算:要制取13g乙炔气体,需要碳化钙的质量。
李老师要用含杂质质量分数为20%的大理石与足量的稀盐酸反应,制备20瓶二氧化碳气体。已知:①集气瓶的体积为100 mL;②大理石中杂质不与稀盐酸反应;
③常温常压下二氧化碳的密度为1.98 g/L。计算李老师需要准备大理石的最少质量。
用于发射天宫一号的长征二号火箭使用的燃料是偏二甲肼(C2H8 N2),用四氧化二氮(N2O4)助燃。该反应的化学方程式为C2H8N2+ 2N2O4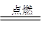 2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?
2CO2↑+ 4H2O + 3N2↑ 计算完全燃烧30 t偏二甲肼会产生多少吨水?