在一定条件下,恒容的密闭容器中发生如下反应:2SO2 (g)+O2(g) 2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是( )
2SO3(g),反应过程中某一时刻测得SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,当反应达到平衡时,可能出现的数据是( )
| A.C(SO3)=0.4mol·L-1 | B.C(SO3)=C(SO2)="0.15" mol·L-1 |
| C.C(O2)=0.3mol·L-1 | D.C(SO3)+C(SO2)="0.4" mol·L-1 |
在100 mL HNO3和H2SO4混合溶液中,两种酸物质的量浓度之和为0.60 mol/L。向该溶液中加入足量的铜粉,加热,充分反应后,所得溶液中Cu2+的物质的量浓度最大为
| A.0.225 mol/L | B.0.36 mol/L | C.0.30 mol/L | D.0.45 mol/L |
茶叶中铁元素检验可用以下步骤完成,各步骤选用实验用品不能都用到的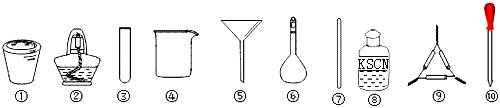
| A.将茶叶灼烧灰化,选用①、②和⑨ |
| B.过滤得到滤液,选用④、⑤和⑦ |
| C.用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ |
| D.检验滤液中的Fe3+,选用③、⑧和⑩ |
下列有关物质组成、性质和用途的说法,正确的是
| A.钠、钾合金(液态)可用于原子反应堆的导电材料 |
| B.煤是由有机物和少量无机物组成的复杂混合物,主要含有苯 |
| C.氮化硅、光导纤维、氧化铝陶瓷等属于新型无机非金属材料 |
| D.化学纤维是把合成纤维经过化学处理得到的高分子材料 |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g) 2NH3(g)△H=-92.4kJ/mol)
2NH3(g)△H=-92.4kJ/mol)
| 容器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
1mol N2、3mol H2 |
2mol NH3 |
4mol NH3 |
| NH3的浓度(mol·L-1) |
c1 |
c2 |
c3 |
| 反应的能量变化 |
放出akJ |
吸收bkJ |
吸收ckJ |
| 体系压强(Pa) |
p1 |
p2 |
p3 |
| 反应物转化率 |
α1 |
α2 |
α3 |
下列说法正确的是
A.2 c1>c3 B.a+b=92.4 C.2 p1<p3 D.α1+α2>1
在pH相同,体积相等的盐酸A和醋酸溶液B中,分别加入等质量的锌,若反应停止后,有一份溶液中锌有剩余,则正确的判断是
①反应所需时间B>A ②开始时反应速度A>B ③参加反应的锌的质量B>A
④整个反应阶段平均速率B>A ⑤盐酸中锌有剩余 ⑥乙酸溶液中锌有剩余
⑦盐酸中放氢气多 ⑧乙酸溶液中放氢气多
| A.③④⑤⑧ | B.①③⑥⑦ | C.①②③⑥ | D.②③④⑤ |