向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体配成溶液逐渐加入盐酸溶液(如图),则原白色固体的成分是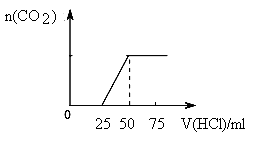
A.NaOH和Na2CO3 B.Na2CO3 C.Na2CO3和NaHCO3 D.NaHCO3
少量铁片与l00 mL 0.01 mol/L的稀盐酸反应,反应速率太慢。为了加快此反应速率而不改变H2的产量,可以使用如下方法中的
①加H2O ②加KNO3溶液 ③滴入几滴浓盐酸 ④加入少量铁粉 ⑤加NaCl溶液
⑥滴入几滴硫酸铜溶液 ⑦升高温度(不考虑盐酸挥发) ⑧改用10 mL 0.1 mol/L盐酸
| A.①⑥⑦ | B.③⑤⑧ | C.③⑦⑧ | D.③④⑥⑦⑧ |
下列递变情况中不正确的是
| A.HF、HCl、HBr、HI的沸点依次升高 |
| B.硅、磷、硫、氯元素的最高正化合价依次升高 |
| C.O2-、F-、Na+、Mg2+的离子半径依次增大 |
| D.锂、钠、钾、铷的金属性依次增强 |
运用元素周期律分析下列推断,其中错误的是
| A.铍是一种轻金属,它的氧化物的水化物可能具有两性 |
| B.砹单质是一种有色固体,砹化氢很不稳定 |
| C.硒化氢(H2Se)是无色、有毒、比H2S稳定的气体 |
| D.硫酸锶难溶于水 |
两种微粒含有相同的质子数和电子数,这两种微粒的关系可能是:(1)同一元素的不同原子,(2)不同元素的原子,(3)两种不同的分子,(4)一种原子和一种分子,(5)一种原子和一种离子,(6)一种分子和一种离子,(7)两种不同的阳离子,(8)两种不同的阴离子,(9)一种阴离子和一种阳离子,其中正确的是
| A.(1)(3)(4)(7)(8) | B.(1)(2)(5)(7)(9) |
| C.(1)(2)(5)(7)(9) | D.(1)(2)(3)(4)(5) |
能与Na反应放出H2,又能使溴水褪色,但不能使pH试纸变色的物质是
| A.CH2=CH—COOH | B.CH2=CH—CH2OH |
| C.CH2=CH—CH3 | D.CH2=CH—COOCH3 |