Na2FeO4是一种高效多功能水处理剂,应用前景广阔。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4 + 6Na2O2 = 2Na2FeO4 + 2Na2O + 2Na2SO4 + O2↑,对此反应下列说法中正确的是( )
| A.Na2O2在反应中只作氧化剂 |
| B.Na2FeO4既是氧化产物又是还原产物 |
| C.O2是还原产物 |
| D.2mol FeSO4发生反应时,反应中共有8mol电子转移 |
短周期元素W、X、Y和Z的原子序数依次增大,金属W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍。下列说法正确的是
A.由金属W制备的高效电池可用 溶液作电解质 溶液作电解质 |
| B.元素Y、Z的最高价氧化物对应水化物之间可以发生反应 |
| C.元素X、Z形成的化合物为离子化合物 |
D.四种元素原子半径由大到小的顺序为: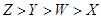 |
用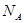 表示阿伏加德罗常数的值。下列叙述中不正确的是
表示阿伏加德罗常数的值。下列叙述中不正确的是
A.足量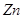 与一定量的浓硫酸反应,产生 与一定量的浓硫酸反应,产生 (标况)气体时,转移的电子数为 (标况)气体时,转移的电子数为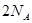 |
B.一定条件下,32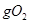 和足量的铁粉充分反应,转移的电子数为 和足量的铁粉充分反应,转移的电子数为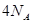 |
C.4.6g乙醇和甲酸(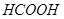 )的混合物中含有的碳原子数在 )的混合物中含有的碳原子数在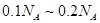 之间 之间 |
D.分子总数为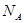 的NO和 的NO和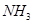 混合气体中含有的氮原子数为 混合气体中含有的氮原子数为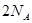 |
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
| a |
b |
c |
|
| A |
 |
 |
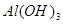 |
| B |
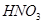 |
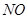 |
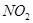 |
| C |
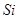 |
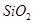 |
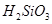 |
| D |
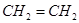 |
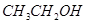 |
 |
下列说法正确的是
A.同温同压下, 在光照和点燃条件下的 在光照和点燃条件下的 不同 不同 |
B.反应: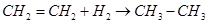 ; ; ,使用和未使用催化剂时,反应热不同 ,使用和未使用催化剂时,反应热不同 |
C.用硝酸这一种试剂就能将 、 、 、Na2CO3、 、Na2CO3、 四种溶液鉴别出来 四种溶液鉴别出来 |
| D.依据丁达尔现象就可将分散系分为溶液、胶体与浊液 |
下列有关化学用语表示正确的是
A.中子数为20的氯原子,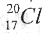 |
B.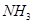 分子的电子式: 分子的电子式: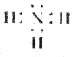 |
C.铝离子结构示意图: |
D.比例模型 表示甲烷分子或四氯化碳分子 表示甲烷分子或四氯化碳分子 |