一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:
MgSO4(s) + CO(g)  MgO(s) + CO2(g) +SO2(g) △H>0
MgO(s) + CO2(g) +SO2(g) △H>0
该反应在恒容的密闭容器中达到平衡后,若仅改变图中横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势合理的是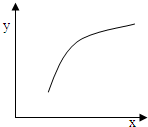
| 选项 |
x |
y |
| A |
温度 |
容器内混合气体的密度 |
| B |
CO的物质的量 |
CO2与CO的物质的量之比 |
| C |
SO2的浓度 |
平衡常数K |
| D |
MgSO4的质量(忽略体积) |
CO的转化率 |
向一个小烧杯中加入20克蔗糖,加3~4滴水,再加入20ml浓硫酸,观察到的实验现象是:烧杯发热、蔗糖变黑、体积膨胀,变成疏松多孔的海棉状的炭,并放出有制激性气味的气体。这个过程中浓硫酸没有表现出的性质是( )
| A.吸水性 | B.脱水性 | C.强氧化性 | D.酸性 |
下列离子方程式正确的是( )
| A.实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O |
| B.氯气与水反应:Cl2+H2O=2H++Cl-+ClO- |
| C.氯化铝溶液加入氨水:Al3++3OH-=Al(OH)3↓ |
D.用氢氧化钠检验氯化铵溶液中铵根离子:NH4++OH― NH3↑+H2O NH3↑+H2O |
下列结论可靠的是( )
A.试液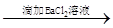 白色沉淀 白色沉淀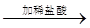 沉淀不溶解 结论:试液中一定含SO42- 沉淀不溶解 结论:试液中一定含SO42- |
B.气体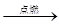 无色气体 无色气体 白色沉淀结论:原气体一定是CO 白色沉淀结论:原气体一定是CO |
C.溶液 冒白雾 冒白雾 白烟结论:原溶液一定是浓盐酸 白烟结论:原溶液一定是浓盐酸 |
D.有色溶液 变红色结论:原溶液中一定含Fe3+ 变红色结论:原溶液中一定含Fe3+ |
下列反应的离子方程式正确的是( )
| A.铁和稀盐酸反应2Fe+6H+=2Fe3++3H2↑ |
| B.碳酸钙溶于稀盐酸中 CO32-+2H+=CO2↑+H2O |
| C.碳酸氢钠溶液与盐酸反应HCO3-+H+=CO2↑+H2O |
| D.氧化铜与盐酸反应 O2―+2H+=H2O |
下列五种有色溶液与SO2作用,均能褪色,其反应实质相同的是( )
①品红溶液②酸性KMnO4溶液③溴水④滴入酚酞的烧碱溶液⑤淀粉—碘溶液
| A.①②③ | B.②③④ | C.③④⑤ | D.②③⑤ |