在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应
X(g)+Y(g) 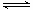 2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g) △H < 0, 一段时间后达到平衡,反应过程中测定的数据如下表:
| t/min |
2 |
4 |
7 |
9 |
| n(Y)/mol |
0.12 |
0.11 |
0.10 |
0.10 |
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
下列关于反应速率的说法中,错误的是( )
| A.反应速率可衡量化学反应的快慢 |
| B.决定反应速率的主要因素是反应物的性质 |
| C.可逆反应达到化学平衡时,正、逆反应速率都为0 |
| D.增大反应物浓度、提高反应物温度都能增大反应速率 |
Cu—Zn稀硫酸组成原电池装置,当导线中有0.5mol电子通过时,理论上两极的变化是( )
①锌极反应:Zn-2e-=Zn2+,锌片上产生0.25mol的H2
②铜极反应:2H++2e-=H2↑,锌片溶解16.25g
③电流由铜极经导线流向锌极
④溶液中SO42-移向铜极
| A.①④ | B.③④ | C.②③ | D.①③ |
燃料电池是燃料(如H2、CO、CH4等)跟氧气或空气起反应,将化学能转变为电能的装置,电解液为强碱溶液。下列关于甲烷燃料电池的说法正确的是( )
| A.负极反应为CH4+10OH-→CO32-+7H2O+8e- |
| B.负极反应为O2+2H2O+4e-→4OH- |
| C.随着放电进行,溶液中的阳离子向负极移动 |
| D.随着放电进行,溶液的PH不变 |
Mg-H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是( )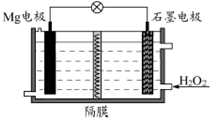
| A.Mg电极是该电池的正极 |
| B.H2O2在石墨电极上发生氧化反应 |
| C.石墨电极附近溶液的pH增大 |
| D.溶液中Cl-向正极移动 |
如图所示装置,电流表G发生偏转,同时X极逐渐变粗,Y极逐渐变细,Z是电解质溶液,则X、Y、Z应是下列各组中的( )
| A.X是Zn,Y是Cu,Z为稀H2SO4 |
| B.X是Cu,Y是Zn,Z为稀H2SO4 |
| C.X是Fe,Y是Ag,Z为稀AgNO3溶液 |
| D.X是Ag,Y是Fe,Z为稀AgNO3溶液 |