下列说法正确的是
| A.实验室从海带提取单质碘的方法依次是:取样、灼烧、溶解、过滤、萃取 |
| B.氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中 |
| C.用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 |
| D.油脂在碱性条件下的水解反应称为油脂的氢化,又称为油脂的硬化 |
下列实验方案中,不能测定Na2CO3和NaHCO3混合物中Na2CO3质量分数的是( )
| A.取a克混合物充分加热,减重b克 |
| B.取a克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得b克固体 |
| C.取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰吸收,增重b克 |
| D.取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
过氧化钠可作为氧气的来源。常温常压下二氧化碳与过氧化钠反应后,若固体质量增加了28 g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数)( )
| 二氧化碳 |
碳酸钠 |
转移的电子 |
|
| A |
1mol |
NA |
|
| B |
22.4L |
1mol |
|
| C |
53g |
1mol |
|
| D |
106g |
2NA |
某溶液中含有较大量的Cl—、CO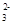 、OH—三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次沉淀出来,下列实验操作顺序正确的是( )
、OH—三种阴离子,如果只取一次该溶液就能够分别将三种阴离子依次沉淀出来,下列实验操作顺序正确的是( )
①滴加Mg(NO3)2溶液 ②过滤③滴加AgNO3溶液④滴加Ba(NO3)2溶液
| A.①②④②③ | B.④②③②① | C.①②③②④ | D.④②①②③ |
对下列实验现象的原因分析不正确的一项是 ()
| 选项 |
实验现象 |
原因分析 |
| A |
浓硫化钠溶液有臭味 |
硫 硫离子水解生成硫化氢,硫化氢具有臭味 |
| B |
新新制氯水中滴加石蕊试液,溶液先变红,后褪色 |
氯气与水反应生成HCl、HClO,HCl显强酸性,使石蕊变红,HClO具有强氧化性,使其褪色 |
| C |
SO 2通入溴水中,溴水褪色 |
SO 2具有漂白性,使其褪色 |
| D |
向向饱和Na2CO3溶液中通入足量CO2气体,溶液变浑浊 |
析析出了NaHCO3晶体 |
下列说法正确的是 ( )
| A.因SiO2不溶于水,故H2SiO3不是SiO2对应的酸,或者说SiO2不是H2SiO3的酸酐 |
| B.CO2通入水玻璃(Na2SiO3溶液)可以得到硅酸 |
| C.因为高温时SiO2与Na2CO3反应生成CO2,故硅酸的酸性比碳酸强 |
| D.因为NH3·H2O是弱碱,所以不能用氨水与FeCl3溶液反应制取Fe(OH)3 |