下列有关电解质溶液的说法正确的是
| A.在蒸馏水中滴加浓H2SO4,KW不变 |
| B.CaCO3难溶于稀硫酸,也难溶于醋酸 |
| C.在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-) |
| D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
在密闭容器中进行反应CH4(g)+H2O(g) CO(g)+3H2(g) ΔH >0,测得c(CH4) 随反应时间(t)的变化如图所示。下列判断正确的是
CO(g)+3H2(g) ΔH >0,测得c(CH4) 随反应时间(t)的变化如图所示。下列判断正确的是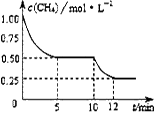
| A.0~5 min内,v(H2)=0.1 mol·(L·min)-1 |
| B.反应进行到12min时,CH4的转化率为25% |
| C.恒温下,缩小容器体积,平衡后H2浓度减小 |
| D.10 min时,改变的外界条件可能是升高温度 |
MCFC型燃料电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。已知该电池的总反应为2H2+O2=2H2O,则下列有关该电池的说法正确的是
| A.该电池的正极反应式为4OH-+4e-=O2+2H2O |
| B.该电池的负极反应式为H2+CO32--2e-=H2O+CO2 |
| C.放电时CO32-向正极移动 |
| D.该燃料电池能量转化率很低 |
在25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是
| A.c(NH4+)=c(SO42-) | B.c(NH4+)>c(SO42-) |
| C.c(NH4+)<c(SO42-) | D.c(OH-) + c(SO42-)=c(H+) + c(NH4+) |
一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如下图所示。下列说法不正确的是
| A.在0点时,醋酸不导电 |
| B.a、b、c三点,a点时醋酸溶液中H+ 浓度最小 |
| C.b点时,醋酸电离程度最大 |
| D.可通过微热的方法使c点溶液中c(CH3COO—) 增大 |
常温下,下列各组离子或分子在指定溶液中能大量共存的是
| A.甲基橙呈红色的溶液中:MnO4-、Al3+、C2H5OH、SO42- |
| B.水电离出的c(H+)=1×10-14 mol·L-1的溶液中:Ca2+、NH4+、Cl-、SiO32- |
| C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、ClO- |
| D.c(NaHCO3)=0.1 mol·L-1的溶液中:K+、C6H5O-、SO42-、CO32- |