【化学——选修3:物质结构与性质】已知A、B、C、D、E五种元素的核电荷数依次增大,除E为第四周期元素外,其余都是短周期元素。其中A、B、C是同一周期的非金属元素,A元素最外层电子数是内层电子数的2倍,B元素基态原子的最外层有3个未成对电子,化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构,E元素的正三价离子的3d亚层为半充满状态。请根据上述情况,回答下列问题(答题时,A、B、C、D、E用所对应的元素符号表示):
(1)元素B、C的第一电离能的大小关系是 (用元素符号填写),其原因为 。
(2)A的的某种氢化物A2H2分子的空间构型是 ,其中心A原子采取的杂化形式为 ,分子中含有 个 键, 个
键, 个 键。
键。
(3)写出E原子的核外电子排布式是 ,用电子式表示化合物DC的形成过程 。
(4)由E元素形成的金属的晶胞结构如图,已知该晶胞边长为a厘米,该晶体的密度为 。(用NA表示阿伏伽德罗常数的值)
(5)配合物E(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此判断E(CO)5晶体属于 (填晶体类型)。
以氯化钾和钛白厂的副产品硫酸亚铁为原料生产硫酸钾、过二硫酸铵和氧化铁红颜料, 原料的综合利用率较高。其主要流程如下:
(1)反应I前需在
溶液中加入(填字母),以除去溶液中的
。
| A. | 锌粉 | B. | 铁屑 | C. | 溶液 | D. |
(2)反应I需控制反应温度低35℃,其目的是。
(3)工业生产上常在反应Ⅲ的过程中加入一定量的醇类溶剂,其目的是:。
(4)反应Ⅳ常被用于电解生产
(过二硫酸铵)。电解时均用惰性电极,阳极发生的电极反应可表示为:。
医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量
、
、
等杂质)生产医药级二水合氯化钙(
的质量分数为97.0%~103.0%)的主要流程如下:
(1)除杂操作是加入氢氧化钙,调节溶液的
为8.0~8.5,以除去溶液中的少量
、
。检验
是否沉淀完全的实验操作是。
(2)酸化操作是加入盐酸,调节溶液的
为4.0,其目的有:①将溶液中的少量
转化为
;②防止
在蒸发时水解;③。
(3)测定样品中
含量的方法是:
a.称取0.7500 样品,溶解,在250 容量瓶中定容;
b.量取25.00 待测液于锥形瓶中;
c.用0.05000
溶液滴定至终点,消耗
溶液体积的平均值为20.39
。
①上述测定过程中需用溶液润洗的仪器有:。
②计算上述样品中
的质量分数为:。
③若用上述方法测定的样品中
的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:;。
现有aA、bB、cC、dD、eE五种短周期元素,它们都是生物体不可缺少的重要元素。已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e,B、D、E都有多种同素异形体。人类已知的化合物中,有一类化合物的种类已超过三千万种,这类化合物中一般都含有A、B两种元素。根据以上信息回答下列有关问题:
(1)请写出下列元素的元素符号: B_____________ D____________ E___________。
(2)写出B、D两元素组成的非极性分子的电子式___________________。
(3)写出由上述五种元素中的四种元素组成的离子化合物的化学式(写出2种即可)
_______________________________、________________________________。
(4)在A、B、D三种元素中选择2种或3种元素,组成2种可发生反应的阴离子,请写出该反应的离子方程式:_________________________________________。
三种短周期元素X、Y、Z两两之间可形成原子个数比均为1:1的三种化合物A、B、C。已知A、B均为离子晶体,构成A晶体的阴离子X-和构成B晶体的阳离子Z+分别与He和Ne具有相同的核外电子排布,常温下,A、B与水都能发生剧烈反应,分别生成无色气体R和W;由X、Y两元素组成的化合物C的水溶液中加入少量MnO2,也发生剧烈反应,放出气体W。据此回答:
(1)Y是(填元素名称)
(2)向C的水溶液中滴入紫色石蕊试液充分振荡后石蕊试液褪色,说明C具有性。
(3)化合物B的电子式为
(4)写出A与水反应的化学方程式
实验室里有一瓶KCl与CaCl2的固体混合物,通过下面实验可确定该混合物中KCl和CaCl2的质量比,也可制得纯净的KCl,根据实验步骤填写下列空白: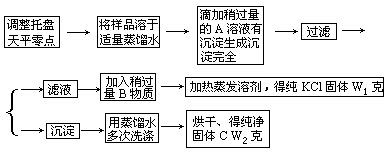
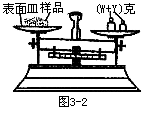 (1) 某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如下图示。请补完整后面的操作是_______。
(1) 某学生用已知质量y克的表面皿,准确称取W克样品,他在托盘天平的右盘放入(W+y)克砝码,在左盘的表面皿中加入样品,这时指针偏向右边,如下图示。请补完整后面的操作是_______。
(2)滤液中加入的B物质是_______,应该加
入过量B物质,理由是_____。
(3)过滤得到沉淀C时,为检验沉淀是否洗净,
应用蒸馏水多次洗涤后,在最后几滴滤出
液中加入______,若______,表示沉淀已洗净。
(4)配制100mL0.20mol·L-1的KCl溶液:某学生用托盘天平将准确称取的(A)1.500gKCl固体放入烧杯中,加入(B)约30mL蒸馏水,用玻璃棒搅拌使其溶解,冷却到室温后,(C)将KCl溶液由烧杯小心倒入100mL容量瓶(不漏液)中,(D)然后往容量瓶中加蒸馏水,直到液面接近标线1—2cm处,摇匀并静置几分钟后,改用胶头滴管加蒸馏水,(E)使溶液凹面最低点恰好与刻度相切,把容量瓶盖盖好,振荡摇匀后装瓶。该学生操作中错误的是_____(填写编号)。
(5)下面哪些操作会导致所配的100mL0.20mol·L-1的KCl溶液浓度降低_________。
(A)容量瓶用蒸馏水洗涤三次直到洗净
(B)称量KCl固体时将砝码放在左盘
(C)未洗涤转移KCl溶液的烧杯
(D)转移KCl溶液时有KCl溶液溅出
(E)定容时仰视刻度线