质量一定时,下列各组有机物不论按何种比例混合后完全燃烧,生成二氧化碳的质量不变的一组物质是 ( )
| A.丙酸和甲酸乙酯 | B.甲醇和乙醇 | C.甲醇和乙酸 | D.乙醇和乙醚 |
如图是课外活动小组的同学设计的4个喷泉实验方案。下列有关操作不可能引发喷泉现象的是
| A.挤压装置①的胶头滴管使CC14全部进入烧瓶,片刻后打开止水夹 |
| B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹 |
| C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹 |
| D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹 |
下列有关物质的结构、分类与性质的说法正确的是
| A.O3和H2O2的分子内都含有共价键 |
| B.2H十的酸性比1H十的酸性更强 |
| C.H216O、D216O、H218O、D218O互为同素异形体 |
| D.O4、O3和O2互为同位素 |
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
| A.16.9g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2NA |
| B.常温常压下,28 g乙烯和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA |
| C.a g某气体含分子数为b,cg该气体在标况下的体积为22.4bc/(aNA)L |
| D.某密闭容器盛有0.1mo1lN2和0.3mo1H2,在一定条件下充分反应,转移电子的数目为0.6NA |
以下说法:①福尔马林和纯盐酸都是混合物:②沼气和核能都是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和建筑用螺纹钢都是合金;⑤臭氧层的破坏和空气液化制取氮气都是发生物理变化;⑥氯水使红墨水褪色原理和NH4HSO3溶液使KMnO4溶液褪色原理相同;⑦豆浆和雾都是胶体。上述说法正确的是
| A.①②③④ | B.①②⑤⑥ | C.③⑤⑥⑦ | D.①③④⑦ |
下图是CO2电催化还原为CH4的工作原理示意图。下列说法不正确的是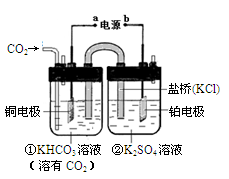
| A.该过程是电能转化为化学能的过程 |
| B.铜电极的电极反应式为:CO2+8H++8e-=CH4+2H2O |
| C.一段时间后,①池中n(KHCO3)不变 |
| D.一段时间后,②池中溶液的pH一定下降 |