某短周期元素原子的最外层电子数是其电子层数的2倍,则下列有关说法正确的是
| A.该元素是金属元素 | B.该元素的最高价氧化物的水化物一定是强酸 |
| C.该元素可能位于第一周期 | D.该元素只有+2和+4两种常见化合价 |
常温下,下列表述正确的是
| A.pH=3的CH3COOH溶液的浓度小于pH=2的盐酸的浓度 |
| B.向NaHCO3溶液中加入少量NaOH固体,可抑制HCO3-的水解,使c(HCO3-)增大 |
| C.将任意量的CH3COOH溶液与NaOH溶液混合,其混合溶液均存在:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
| D.Na2CO3溶液中:c(Na+)>c(CO32-)>c(OH-)=c(HCO3-)>c(H+) |
下列实验操作、现象和结论均正确的是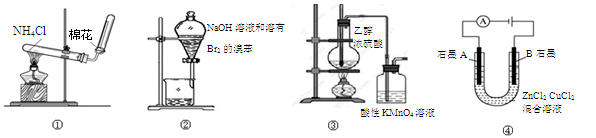
| 选项 |
操作 |
现象 |
结论 |
| A |
①将湿润的红色石蕊试纸靠近试管口 |
试纸不变色 |
NH4Cl受热不分解 |
| B |
②中振荡后静置 |
下层液体颜色变浅 |
NaOH溶液可除去溶在溴苯中的Br2 |
| C |
③加热 |
洗气瓶中溶液褪色 |
生成了乙烯 |
| D |
④通电 |
A极上有红色固体析出 |
不能说明锌的金属性比铜强 |
下列说法正确的是
①标准状况下,2.24 LNO2与水反应生成NO3-的数目为0.1NA
②质子数为92、中子数为143的铀(U)原子: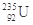
③向苯酚钠溶液中通入少量的CO2:CO2 + H2O + 2C6H5O- 2C6H5OH + 2CO32-
2C6H5OH + 2CO32-
④在由水电离出的c(OH-)=10-13 mol·L-1的溶液中:Na+、Ba2+、Cl-、I-可大量共存
⑤0.1 mol溴苯中含有双键的数目为0.3NA
⑥1,3—二甲基丁烷: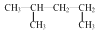
| A.①②⑤ | B.②④⑥ | C.②④ | D.③⑤⑥ |
下列有关说法中,正确的是
| A.光导纤维、聚酯纤维、棉花都属于有机高分子化合物 |
| B.在大米酿酒的过程中,淀粉最后变成了单糖 |
| C.“地沟油”经过加工处理后可以用来制肥皂 |
| D.明矾和漂白粉处理自来水,二者的作用原理相同 |
化学与社会、生产、生活紧切相关。下列说法正确的是
| A.棉花和木材的主要成分都是纤维素,蚕丝和人造丝的主要成分都是蛋白质 |
| B.石油干馏可得到石油气、汽油、煤油、柴油等 |
| C.从海水中提取物质都必须通过化学反应才能实现 |
| D.纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污 |