某温度下,在一个2 L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A(g)+2B(g)  4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?)。反应一段时间后达到平衡,测得生成1.6 mol C,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A.该反应的化学平衡常数表达式是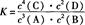 |
| B.此时,B的平衡转化率是35% |
| C.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
| D.增大C,B的平衡转化率不变 |
已知2SO2+O2  2SO3为放热反应,对该反应的下列说法中正确的是
2SO3为放热反应,对该反应的下列说法中正确的是
| A.O2的能量一定高于SO2的能量 | B.SO2和O2的总能量一定高于SO3的总能量 |
| C.SO2的能量一定高于SO3的能量 | D.因该反应为放热反应,故不必加热就 可发生 可发生 |
两种元素可以组成AB2型离子化合物,它们的原子序数可能是
A 11和8 B 6和8 C 7和8 D 12和9
人造地球卫星用的一 种高能电池——银锌电池,器
种高能电池——银锌电池,器 电池的电极反应式为:
电池的电极反应式为:
Zn+2OH- -2e- = ZnO+H2O;Ag2O+H2O+2e-=2Ag+2OH-,据此判断氧化银是
| A.负极,并被氧化 | B.正极,并被还原 |
| C.负极,并被还原 | D.正极,并被氧化 |
在一定温度下,可逆反应A(气)+3B(气) 2C若达到平衡的标志是
2C若达到平衡的标志是
| A.C的生成速率与B的生成速率相等 | B.A、B、C的浓度不再发生变化 |
| C.A、B、C的分子数之比为1∶3∶2 | D.单位时间内生成A n mol,同时生成B 3n mol |
下列递变规律 正确的是
正确的是
A.O、S、Na、K的原子半径依次增大
B.Na、Mg、Al、Si的金属性逐渐增强
C.HF、HCl、H2S、PH3的稳定性依次增强
D .KOH、Ca(OH
.KOH、Ca(OH )2、Mg(OH)2、Al(OH)3的碱性逐渐增强
)2、Mg(OH)2、Al(OH)3的碱性逐渐增强