已知25℃、101 kPa时,乙烯和乙炔(C2H2)燃烧的热化学方程式分别为 ΔH=一1411 kJ/mol
ΔH=一1411 kJ/mol ΔH=一2600 kI/mol
ΔH=一2600 kI/mol
又知燃烧时火焰的温度乙炔高于乙烯。据此,下列说法不正确的是 ( )
| A.物质的燃烧热越大,火焰温度越高 |
| B.相同条件下等体积乙烯和乙炔完全燃烧时,乙炔放热较少 |
| C.25℃、101 kPa时,1 mol乙烯完全燃烧生成气态产物时,放出的热量小于1411 kJ |
| D.乙炔的燃烧热为1300 kJ/mol |
设NA表示阿伏加德罗常数,下列说法中不正确的是
| A.0.5mol O3和11.2L O2的体积一定相等 |
| B.5.6 gFe与足量的稀盐酸充分反应后,转移的电子数为0.2NA |
| C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D.1L 0.1mol/L的醋酸溶液中H+数目为0.1 NA |
为了有效除去工业食盐中的Ca2+、Mg2+、SO42—,加入试剂的合理顺序为
| A.先加NaOH,后加Na2CO3,再加BaCl2 |
| B.先加NaOH,后加BaCl2,再加Na2CO3 |
| C.先加BaCl2,后加NaOH,再加Na2CO3 |
| D.先加Na2CO3,后加BaCl2溶液,再加NaOH |
在酸性溶液中,下列各组离子能大量共存的是
| A.Cl-、HCO3-、K+、SO42- | B.OH-、Cl-、Na+、Mg2+ |
C.Fe3+、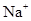 、SO32-、I- 、SO32-、I- |
D.Na+、Cl-、I-、SO42- |
能正确表示下列反应的离子方程式是
| A.钠投入水中:Na+H2O=Na++OH-+H2↑ |
| B.碳酸钙与醋酸反应:CO32-+2CH3COOH===CO2↑+H2O+2CH3COO- |
| C.少量碳酸氢钙溶液与足量氢氧化钠溶液反应:Ca2+ + HCO3-+ OH-= CaCO3 ↓ + H2O |
| D.铜片插入硝酸银溶液中:Cu +2Ag+= Cu2++2Ag |
M2O7X-与S2-在酸性溶液中反应如下:M2O7X-+3S2-+14H+=2M3++3S↓+7H2O,则M2O7X-中M的化合价是
| A.+2 | B.+3 | C.+4 | D.+6 |