丙烯酸(CH2===CH—COOH)的性质可能有( )
①加成反应 ②取代反应 ③酯化反应 ④中和反应 ⑤氧化反应
| A.①③ | B.①③④ | C.①③④⑤ | D.①②③④⑤ |
在下列给定条件的溶液中,一定能大量共存的离子组是
| A.澄清透明溶液:H+、Na+、SO42-、C6H5O- |
| B.常温下Kw/c(H+)=0.1 mol/L的溶液:K+、Na+、SiO32-、NO3- |
| C.铁片加入产生气泡的溶液:Na+、NH4+、I-、NO2- |
| D.NaHCO3溶液:K+、Na+、SO42-、Al3+ |
某含Na+的溶液中可能含有NH4+、Fe3+、Br—、CO32—、I—、SO32—。取样,滴加足量氯水,有气泡产生,溶液呈橙色;向橙色溶液中加BaCl2溶液或淀粉均无现象。为确定该溶液的组成,还需进行的实验有
| A.取样,滴加硫氰化钾溶液 |
| B.取样,加氯水和CCl4,振荡 |
| C.取样,加足量盐酸加热,湿润的品红试纸检验气体 |
| D.取样,加足量的熟石灰加热,湿润的红色石蕊试纸检验气体 |
已知:H2(g)+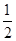 O2(g)=H2O(l)ΔH1=-285.8 kJ·mol-1 ①
O2(g)=H2O(l)ΔH1=-285.8 kJ·mol-1 ①
H2(g)=H2(l) ΔH2=-0.92 kJ·mol-1②O2(g)=O2(l)ΔH3=-6.84 kJ·mol-1③
H2O(g)=H2O(l)ΔH4=-44 kJ·mol-1④
下列说法正确的是
| A.上述四个反应都是吸热反应 |
| B.1 mol液态H2的能量大于1 mol气态H2的能量 |
| C.H2的燃烧热(ΔH)为-285.8 kJ·mol-1 |
D.火箭中液氢燃烧的热化学方程式为H2(l)+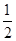 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 O2(l)=H2O(g) ΔH=-285.8 kJ·mol-1 |
下列有关物质的性质与应用不相对应的是
| A.二氧化硫具有漂白性,可用于漂白纸浆 | B.常温下,铝能被浓硫酸钝化,可用铝罐贮运浓硫酸 |
| C.MgO熔点很高,可用于制作耐火材料 | D.氢氟酸具有弱酸性,可用于蚀刻玻璃 |
高温下,某反应达平衡,化学平衡常数表达式为: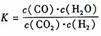 ,恒容时,温度升高H2浓度减小。下列说法正确的是
,恒容时,温度升高H2浓度减小。下列说法正确的是
A.该反应化学方程式为:CO(g)+H2O(g)  CO2(g)+H2(g) CO2(g)+H2(g) |
| B.恒温恒容下,反应达平衡时,再通入一定量的CO2,CO的体积分数一定增大 |
| C.升高温度,正反应速率增大,逆反应速率减小 |
| D.该反应的焓变为正值 |