下列热化学方程式中,△H能正确表示物质的燃烧热的是
| A.2CO(g) +O2(g) ==2CO2(g)△H=—566.0 kJ/mol |
| B.C(s) +1/2O2(g) ==CO(g)△H=—110.5 kJ/mol |
| C.CH4(g) +2O2(g)="=" CO2(g)+2H2O(l)△H=—890.31 kJ/mol |
| D.2C8H18(l) +25O2(g)==16CO2(g)+18H2O(l)△H=—11036 kJ/mol |
下列各对物质中,互为同系物的是
A.CH3-CH=CH2与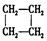 |
B.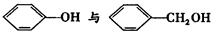 |
| C.甲苯和二甲苯 | D.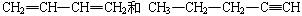 |
下列各化合物的命名中正确的是
| A.CH2=CH-CH=CH2 1,3—二丁烯 | B.CH3 –O –CH3乙醚 |
C.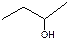 3―丁醇 3―丁醇 |
D.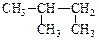 2―甲基丁烷 2―甲基丁烷 |
研究有机物一般经过以下几个基本步骤:分离、提纯→确定实验式→确定分子式→确定结构式,以下用于研究有机物的方法错误的是
| A.蒸馏可用于分离提纯液态有机混合物 |
| B.燃烧法是研究确定有机物成分的一种有效方法 |
| C.核磁共振氢普通常用于分析有机物的相对分子质量 |
| D.对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
2010年下半年,我国接连发生多起煤矿爆炸事故,造成重大人员伤亡和财产损失。煤矿发生爆炸事故的元凶是煤矿坑道气中含有的甲烷。下列关于甲烷的叙述中错误的是
| A.“抽”出坑道中的甲烷,既可用作清洁燃料,又可防止爆炸 |
| B.甲烷分子是一种呈正四面体型的分子 |
| C.甲烷是重要的化工原料,其分解产物可用于合成氨和橡胶工业 |
| D.甲烷分子中两个氢原子被氯取代后,可形成两种不同结构的分子 |
某合金(仅含铜、铁)中铜和铁的物质的量之和为ymol,其中Cu的物质的量分数为a ,将其全部投入100mLbmol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:
| A.b≥40y(2-) | B.b≥8 0y(2-) 0y(2-) |
| C.b≥40y(1-) | D.b≥80y(1-) |