将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表:(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大。)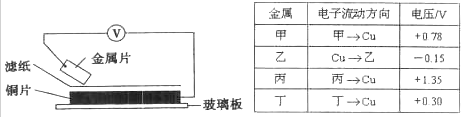
依据记录数据判断,下列结论中正确的是
| A.将甲、乙形成的合金露置在空气中,甲先被腐蚀 |
| B.金属乙能从硫酸铜溶液中置换出铜 |
| C.在四种金属中丙的还原性最弱 |
| D.甲、丁若形成原电池时,甲为正极 |
根据表中信息判断,下列选项不正确的是
| 序号 |
反应物 |
产物 |
| ① |
KMnO4、H2O2、H2SO4 |
K2SO4、MnSO4...... |
| ② |
Cl2、FeBr2 |
FeCl3、FeBr3 |
| ③ |
MnO4-...... |
Cl2、Mn2+...... |
A.第①组反应的其余产物为H2O和 O2
B.第②组反应中Cl2与 FeBr2的物质的量之比小于或等于1︰2
C.第③组反应中生成1mol Cl2,转移电子2mol
D.氧化性由强到弱顺序为MnO4-> Cl2 > Fe3+ > Br2
设NA是阿伏加德罗常数的数值,下列说法不正确的是
| A.1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3 NA |
| B.标准状况下,2.24 L Cl2溶于水,转移的电子数目为0.1NA |
| C.常温常压下,8 g SO3所含的氧原子的数目为0.3NA |
| D.过氧化钠与H2O反应,每生成0.1mol氧气,转移电子的数目为0.2NA |
下列说法不正确的是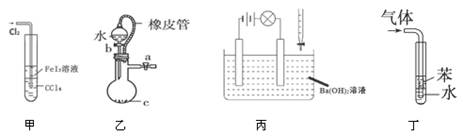
| A.甲装置可以用于比较Fe3+ 、I2、Cl2的氧化性强弱 |
| B.乙装置中橡皮管的作用是使水能顺利流下 |
| C.丙装置中,若向Ba(OH)2溶液中逐滴加入硫酸溶液直至过量,灯光会由亮变暗至熄灭后又逐渐变亮 |
| D.丁装置用于吸收HCl气体能防倒吸 |
下列说法不正确的是
| A.碱金属元素在自然界以化合态形式存在 |
| B.金属铷投入水中会发生爆炸式反应,生成氢氧化铷和氢气 |
| C.碱金属与氧气反应,生成物都不随反应条件或反应物的用量变化而变化 |
| D.金属铯的密度大于钠,而钠的熔点高于铯 |
下列说法正确的是
| A.用铂丝蘸取某盐溶液进行焰色反应,火焰呈黄色,说明该盐溶液含钠元素,一定不含钾元素 |
| B.配制100 mL 1 mol/L NaCl溶液,定容时俯视刻度线,则所配溶液浓度偏小 |
| C.只用胶头滴管和试管,不用其他试剂无法区别稀盐酸和K2CO3稀溶液 |
| D.纳米材料微粒直径一般从几纳米到几十纳米,将纳米材料分散到溶剂中得到的分散系,用可见光束照射具有丁达尔效应 |