下列事实不能用勒沙特列原理解释的是( )
| A.氨水应密闭保存,放置低温处 |
| B.在FeC12溶液中加入铁粉防止氧化变质 |
| C.常温下,将1mLpH=3的醋酸溶液加水稀释至l00mL,测得其pH<5 |
| D.实验室可用排饱和食盐水的方法收集氯气 |
下列实验不合理的是: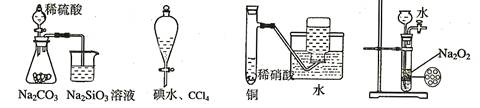
| A.证明非金属性强弱 S>C>Si | B.四氯化碳萃取碘水中的碘 |
| C.制备并收集少量NO气体 | D.制备少量氧气 |
某有机物X的结构简式如下图所示,则下列有关说法中正确的是:
| A.X的分子式为C12H16O3 |
| B.可用酸性高锰酸钾溶液区分苯和X |
| C.X在一定条件下能发生加成、加聚、取代、消去等反应 |
| D.在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成 |
设NA为阿伏加德罗常数的值。下列说法正确的是:
| A.标准状况下,22.4L HF中含HF分子数目为NA |
| B.28g由乙烯和丙烯组成的混合气体中含碳碳双键数目为NA |
| C.71gNa2SO4固体中含钠离子数目为NA |
| D.25g质量分数68%的H2O2水溶液中含氧原子数目为NA |
在环境保护、资源利用等与社会可持续发展密切相关的领域化学发挥着积极作用。下列做法与此理念相违背的是:
| A.食品中大量添加苯甲酸钠等防腐剂,可有效延长其保质期 |
| B.“地沟油”可以制成肥皂,提高资源的利用率 |
| C.加快开发高效洁净能源转换技术,缓解能源危机 |
| D.“A PEC蓝”是2014年新的网络词汇,形容2014年A PEC会议期间北京蓝蓝的天空。说明京津冀实施道路限行和污染企业停工等措施,对减轻雾霾、保证空气质量是有效的 |
下列说法正确的是:
A.将pH均为a的氢氧化钠溶液和氨水分别加水稀释100倍,pH变为b和c,则a、b、c的大小关系是:b>c>a
B.常温下5.0×10-3mol·L-1KHA溶液的pH="3.75" ,该溶液中c(A2-)< c(H2A)
C.室温时,M(OH)2(s)  M2+(aq)+2OH-(aq) Ksp=a;c(M2+)="b" mol·L-1时,溶液的pH等于14+
M2+(aq)+2OH-(aq) Ksp=a;c(M2+)="b" mol·L-1时,溶液的pH等于14+ 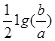
D.Na2C2O4溶液:c(OH-)=c(H+)+c(HC2O4-)+2c(H2C2O4)