已知合成氨反应N2(g)+3H2(g) 2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:
2NH3(g)△H=-92.30kJ ·mol-1,在某温度下,2L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) |
0 |
1 |
2 |
3 |
4 |
| N2 |
1.50 |
n1 |
1.20 |
n3 |
n5 |
| H2 |
4.50 |
4.20 |
3.60 |
n4 |
n6 |
| NH3 |
0 |
0.20 |
n2 |
1.00 |
1.00 |
下列说法正确的是
A.反应进行到1小时时放出的热量为9.23kJ
B.反应3h内,反应速率v(N2)为0.17mol·L-1·h-1
C.此温度下,该反应的平衡常数为0.037
D.4h时,若再加入1mol N2,达到新的平衡时,N2的转化率是原的两倍
下列液体中,不会出现丁达尔效应的是()
①鸡蛋清溶液 ②水③淀粉溶液 ④硫酸钠溶液 ⑤沸水中滴入饱和FeCl3溶液形成的混合物
| A.②④ | B.③④ | C.②④⑤ | D.④ |
一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是()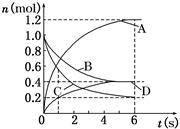
A.反应进行到6 s时,各物质的反应速率相等
B.反应进行到1 s时,v (A)=v (C)
C.反应进行到6 s时,B的平均反应速率为0.1 mol/(L·s)
D.该反应的化学方程式为3B+4 C 6A+2D
6A+2D
已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1
H2(g)+ O2(g)=H2O(l)ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l)ΔH=-285.8 kJ·mol-1
由此可知,在等温下蒸发36 g液态水需吸收的热量()
| A.483.6 kJ | B.88 kJ | C.285.8 kJ | D.44 kJ |
图中,两电极上发生的电极反应为:a极:Cu2++2e—=Cu,b极:Fe—2e一=Fe2+,下列说法中不正确的是()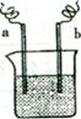
| A.该装置可能是电解池 |
| B.a极上发生的是还原反应 |
| C.a、b不可能是同种电极材料 |
| D.该装置工作时,溶液中的阴离子向b极移动 |
金属镍有广泛的用途。粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+) ( )
| A.阳极发生还原反应,其电极反应式:Ni2++2e-= Ni |
| B.电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
| C.电解过程中,阳极质量的减少与阴极质量的增加不相等 |
| D.电解后,电解槽底部的阳极泥中只有Pt |